Тубулярная грудь — причины, симптомы, диагностика и лечение
Тубулярная грудь – аномалия развития молочных желез, при которой уменьшается площадь их основания, возникает недостаток тканей, альвеолярная грыжа и птоз. В результате вышеперечисленных нарушений грудь приобретает вытянутую «трубчатую» форму и неэстетичный внешний вид. Обычно патология выявляется с двух сторон, реже встречается поражение одной железы. Диагностика производится на основании данных осмотра, в качестве дополнительных методов в рамках предоперационной подготовки используют маммографию. Для коррекции применяют реконструктивные пластические операции с установкой эндопротезов (имплантатов).
Общие сведения
Тубулярная грудь («козья грудь») происходит от латинского слова «tuba» – труба, поскольку вытянутая форма молочных желез на узком основании и с выпирающей ареолой похожа на трубку или цилиндр. Точные данные о распространенности отсутствуют, считается, что состояние выявляется примерно у 20 женщин из тысячи. Сложность определения встречаемости патологии обусловлена относительно редким обращением пациенток за медицинской помощью из-за отсутствия выраженной симптоматики (за исключением эстетического недостатка). Имеется расовая предрасположенность – у лиц негроидной расы подобная аномалия молочных желез регистрируется в несколько раз чаще.
Сложность определения встречаемости патологии обусловлена относительно редким обращением пациенток за медицинской помощью из-за отсутствия выраженной симптоматики (за исключением эстетического недостатка). Имеется расовая предрасположенность – у лиц негроидной расы подобная аномалия молочных желез регистрируется в несколько раз чаще.
Тубулярная грудь
Причины
Непосредственные причины развития данной патологии не установлены. По невыясненным обстоятельствам в тканях молочных желез возникают плотные соединительнотканные перемычки, которые формируют плотную сеть или футляр у основания органов. В процессе полового созревания перемычки растут медленнее, чем жировая и железистая ткань, деформируют железы, изменяют направление их роста в сторону ареолы и соска. С наружной стороны от футляра или сети жировая ткань не растет, что создает визуальную картину дефицита. Существует несколько теорий возникновения заболевания:
- Генетические факторы. Описаны семейные случаи развития тубулярной груди, наследование предположительно происходило по женской линии.
 Не выявлены ключевые гены, ответственные за развитие патологии, точный характер наследования и другие детали.
Не выявлены ключевые гены, ответственные за развитие патологии, точный характер наследования и другие детали. - Тератогенные факторы. Согласно этой гипотезе, аномалия имеет врожденный характер, обусловлена химическими или биологическими воздействиями на внутриутробном этапе развития.
- Приобретенные факторы. Некоторые исследователи отрицают врожденный характер как минимум части случаев порока развития, аргументируя это отсутствием изменений до начала подросткового периода. По их мнению, патология возникает из-за нарушения кровоснабжения тканей молочных желез, обусловленного заболеваниями, ношением неподходящих бюстгальтеров и пр.
Отсутствие точных данных относительно причин аномалии не позволяет заблаговременно выявлять заболевание и производить этиотропное лечение. Существующие гипотезы не объясняют ряд особенностей патогенеза данного состояния, поэтому его изучение продолжается.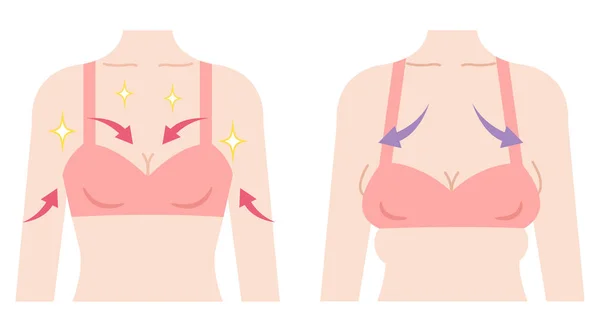
Патогенез
Развитие тубулярной груди начинается в период полового созревания с началом роста молочных желез под влиянием женских половых гормонов и завершается к 17-20 годам. После этого аномалия прогрессирует крайне редко, беременность и кормление грудью лишь незначительно изменяют выраженность нарушения. Некоторые участки соединительнотканной стромы утолщаются и теряют эластичность, формируя плотное кольцо у основания железы. По мере роста девочки из соединительной ткани образуется плотный каркас или футляр, не позволяющий железистым и жировым структурам разрастаться в ширину.
Рост нормальных железистых компонентов возможен только в пределах футляра, поэтому внешне нарушение проявляется как дефицит тканей на внутренней и нижней частях груди или по всей ее поверхности. В тяжелых случаях в процессе роста возникает сдавление тканей, ухудшается кровоснабжение молочных желез, что усиливает процессы склерозирования. У пациенток расширяется область ареолы, развивается состояние, известное как «ареолярная грыжа». В период лактации возможны трудности с кормлением ребенка, обусловленные нарушением питания железистой ткани, аномальной формой и размерами ареолы и соска.
В период лактации возможны трудности с кормлением ребенка, обусловленные нарушением питания железистой ткани, аномальной формой и размерами ареолы и соска.
Классификация
В пластической хирургии выделяют три клинических формы тубулярной груди, отличающиеся степенью выраженности порока и, следовательно, недостатка тканей желез. Эти формы не являются последовательными стадиями аномалии развития.
- Первый тип.
- Второй тип. Значительный недостаток тканей наблюдается в нижних квадрантах. Железа смещается вниз, при осмотре регистрируется расширение ареолы и уплощение соска.
- Третий тип. Формируется соединительнотканный футляр, который сужает основание желез и сильно препятствует их росту.
 Возникает существенный дефицит тканей. Рост тубулярной груди возможен только по направлению к соску, это приводит к резкому расширению сосково-ареолярного комплекса и развитию ареолярной грыжи.
Возникает существенный дефицит тканей. Рост тубулярной груди возможен только по направлению к соску, это приводит к резкому расширению сосково-ареолярного комплекса и развитию ареолярной грыжи.
Симптомы
Тубулярная грудь выявляется при внешнем осмотре. Молочные железы в зависимости от типа аномалии имеют конусовидную или цилиндрообразную форму. Основание органа сужено, что приводит к увеличению межгрудного пространства и птозу желез. Ареолы расширены, часто отмечается их недоразвитость (несоответствие возрасту женщины). Сосок уплощен, может наблюдаться его втягивание и разнообразные аномалии строения. В тяжелых случаях образуется ареолярная грыжа, проявляющаяся выступающим сосково-ареолярным комплексом.
Субъективных симптомов (болей, дискомфорта) при тубулярности обычно не отмечается. В период кормления могут возникать затруднения из-за недостаточного образования молока по причине уменьшенного объема железистой ткани. При нарушении строения сосково-ареолярного комплекса ребенок не может правильно захватить грудь, что ведет к заглатыванию воздуха и дополнительно снижает количество молока.
При нарушении строения сосково-ареолярного комплекса ребенок не может правильно захватить грудь, что ведет к заглатыванию воздуха и дополнительно снижает количество молока.
Осложнения
При отсутствии лечения органические осложнения тубулярной груди не возникают. Имеются отдельные указания на более высокий риск развития мастопатий и связанных с ними нарушений, однако четкой корреляции не выявлено. Пациентки нередко страдают от психологических расстройств – эстетический дефект может стать причиной появления комплексов и развития неврозов. После хирургической коррекции порока иногда формируются гематомы, образуются грубые рубцы, возможно инфицирование операционной раны.
Диагностика
Постановка диагноза не представляет затруднений, осуществляется на основании результатов осмотра маммолога. Специалист определяет размеры и форму молочных желез, выявляет нарушение структуры органа (наличие уплотнений). Дифференциальную диагностику проводят с некоторыми типами мастопатий, особенно при асимметричной груди. Пальпаторное обнаружение уплотнений в структуре желез, втянутость сосков и наличие ареолярной грыжи являются поводом для назначения УЗИ груди и маммографии. Перечисленные исследования также проводятся в период подготовки к операции.
Пальпаторное обнаружение уплотнений в структуре желез, втянутость сосков и наличие ареолярной грыжи являются поводом для назначения УЗИ груди и маммографии. Перечисленные исследования также проводятся в период подготовки к операции.
Коррекция тубулярной груди
Для устранения патологии используют хирургические методы лечения, их характер зависит от выраженности патологического состояния и пожеланий пациентки. Проводить операцию допустимо только при полностью сформированных молочных железах после достижения 22-24 лет. Ранняя коррекция может привести к появлению деформаций и изменению формы груди, для устранения которых потребуются дополнительные вмешательства. В тяжелых случаях (третий тип тубулярной груди) для восстановления эстетичного вида необходимо комплексное хирургическое лечение, общая продолжительность которого может составлять около 1 года.
- Эндопротезирование груди. Для коррекции тубулярности пластические хирурги используют специальную технику установки имплантатов посредством периареолярного доступа.
 Для равномерного распределения паренхимы железы на ее ткань наносят насечки. В некоторых случаях требуется подбор специальных имплантатов для формирования симметричной груди.
Для равномерного распределения паренхимы железы на ее ткань наносят насечки. В некоторых случаях требуется подбор специальных имплантатов для формирования симметричной груди. - Установка тканевого эспандера. Применяется при втором и третьем типах состояния в рамках подготовки к эндопротезированию. Целью вмешательства является растяжение тканей для формирования ложа имплантата. После установки эспандера его наполняют изотоническим раствором, каждые две недели увеличивая объем. Длительность растяжения составляет не менее 2-3 месяцев в зависимости от выраженности недостатка тканей.
- Уменьшение соска и ареолы. Операция может проводиться изолированно (при первом типе тубулярности) или как завершающий этап коррекции в случае более выраженной аномалии. Края ареолы иссекают, оставляя круг диаметром не более 4 сантиметров, и подшивают к коже.
Прогноз
Прогноз для жизни и здоровья при тубулярной груди благоприятный. Иногда отмечаются сложности с грудным вскармливанием, но в большинстве случаев жалобы пациенток связаны с неэстетичным видом груди и вторичными психологическими нарушениями. При коррекции возможны хирургические осложнения (гематомы, келоидные и гипертрофические рубцы, серома), однако их частота сравнительно невелика. В отдаленном периоде после операций может наблюдаться развитие контурирования или смещение имплантата, повреждение его оболочки.
Иногда отмечаются сложности с грудным вскармливанием, но в большинстве случаев жалобы пациенток связаны с неэстетичным видом груди и вторичными психологическими нарушениями. При коррекции возможны хирургические осложнения (гематомы, келоидные и гипертрофические рубцы, серома), однако их частота сравнительно невелика. В отдаленном периоде после операций может наблюдаться развитие контурирования или смещение имплантата, повреждение его оболочки.
Тубулярная грудь — причины, симптомы, диагностика и лечение
Тубулярная грудь – аномалия развития молочных желез, при которой уменьшается площадь их основания, возникает недостаток тканей, альвеолярная грыжа и птоз. В результате вышеперечисленных нарушений грудь приобретает вытянутую «трубчатую» форму и неэстетичный внешний вид. Обычно патология выявляется с двух сторон, реже встречается поражение одной железы. Диагностика производится на основании данных осмотра, в качестве дополнительных методов в рамках предоперационной подготовки используют маммографию.
Общие сведения
Тубулярная грудь («козья грудь») происходит от латинского слова «tuba» – труба, поскольку вытянутая форма молочных желез на узком основании и с выпирающей ареолой похожа на трубку или цилиндр. Точные данные о распространенности отсутствуют, считается, что состояние выявляется примерно у 20 женщин из тысячи. Сложность определения встречаемости патологии обусловлена относительно редким обращением пациенток за медицинской помощью из-за отсутствия выраженной симптоматики (за исключением эстетического недостатка). Имеется расовая предрасположенность – у лиц негроидной расы подобная аномалия молочных желез регистрируется в несколько раз чаще.
Тубулярная грудь
Причины
Непосредственные причины развития данной патологии не установлены. По невыясненным обстоятельствам в тканях молочных желез возникают плотные соединительнотканные перемычки, которые формируют плотную сеть или футляр у основания органов. В процессе полового созревания перемычки растут медленнее, чем жировая и железистая ткань, деформируют железы, изменяют направление их роста в сторону ареолы и соска. С наружной стороны от футляра или сети жировая ткань не растет, что создает визуальную картину дефицита. Существует несколько теорий возникновения заболевания:
В процессе полового созревания перемычки растут медленнее, чем жировая и железистая ткань, деформируют железы, изменяют направление их роста в сторону ареолы и соска. С наружной стороны от футляра или сети жировая ткань не растет, что создает визуальную картину дефицита. Существует несколько теорий возникновения заболевания:
- Генетические факторы. Описаны семейные случаи развития тубулярной груди, наследование предположительно происходило по женской линии. Не выявлены ключевые гены, ответственные за развитие патологии, точный характер наследования и другие детали.
- Тератогенные факторы. Согласно этой гипотезе, аномалия имеет врожденный характер, обусловлена химическими или биологическими воздействиями на внутриутробном этапе развития.
- Приобретенные факторы. Некоторые исследователи отрицают врожденный характер как минимум части случаев порока развития, аргументируя это отсутствием изменений до начала подросткового периода.
 По их мнению, патология возникает из-за нарушения кровоснабжения тканей молочных желез, обусловленного заболеваниями, ношением неподходящих бюстгальтеров и пр.
По их мнению, патология возникает из-за нарушения кровоснабжения тканей молочных желез, обусловленного заболеваниями, ношением неподходящих бюстгальтеров и пр.
Отсутствие точных данных относительно причин аномалии не позволяет заблаговременно выявлять заболевание и производить этиотропное лечение. Существующие гипотезы не объясняют ряд особенностей патогенеза данного состояния, поэтому его изучение продолжается.
Патогенез
Развитие тубулярной груди начинается в период полового созревания с началом роста молочных желез под влиянием женских половых гормонов и завершается к 17-20 годам. После этого аномалия прогрессирует крайне редко, беременность и кормление грудью лишь незначительно изменяют выраженность нарушения. Некоторые участки соединительнотканной стромы утолщаются и теряют эластичность, формируя плотное кольцо у основания железы. По мере роста девочки из соединительной ткани образуется плотный каркас или футляр, не позволяющий железистым и жировым структурам разрастаться в ширину.
Рост нормальных железистых компонентов возможен только в пределах футляра, поэтому внешне нарушение проявляется как дефицит тканей на внутренней и нижней частях груди или по всей ее поверхности. В тяжелых случаях в процессе роста возникает сдавление тканей, ухудшается кровоснабжение молочных желез, что усиливает процессы склерозирования. У пациенток расширяется область ареолы, развивается состояние, известное как «ареолярная грыжа». В период лактации возможны трудности с кормлением ребенка, обусловленные нарушением питания железистой ткани, аномальной формой и размерами ареолы и соска.
Классификация
В пластической хирургии выделяют три клинических формы тубулярной груди, отличающиеся степенью выраженности порока и, следовательно, недостатка тканей желез. Эти формы не являются последовательными стадиями аномалии развития.
- Первый тип. Из-за соединительнотканных перемычек затрудняется рост груди в медиальных и нижних квадрантах с возникновением дефицита тканей.
 Дефект выражен слабо, молочная железа несколько приподнята вверх, ареола и сосок не изменены. Патология часто не требует коррекции.
Дефект выражен слабо, молочная железа несколько приподнята вверх, ареола и сосок не изменены. Патология часто не требует коррекции. - Второй тип. Значительный недостаток тканей наблюдается в нижних квадрантах. Железа смещается вниз, при осмотре регистрируется расширение ареолы и уплощение соска.
- Третий тип. Формируется соединительнотканный футляр, который сужает основание желез и сильно препятствует их росту. Возникает существенный дефицит тканей. Рост тубулярной груди возможен только по направлению к соску, это приводит к резкому расширению сосково-ареолярного комплекса и развитию ареолярной грыжи.
Симптомы
Тубулярная грудь выявляется при внешнем осмотре. Молочные железы в зависимости от типа аномалии имеют конусовидную или цилиндрообразную форму. Основание органа сужено, что приводит к увеличению межгрудного пространства и птозу желез. Ареолы расширены, часто отмечается их недоразвитость (несоответствие возрасту женщины). Сосок уплощен, может наблюдаться его втягивание и разнообразные аномалии строения. В тяжелых случаях образуется ареолярная грыжа, проявляющаяся выступающим сосково-ареолярным комплексом.
Сосок уплощен, может наблюдаться его втягивание и разнообразные аномалии строения. В тяжелых случаях образуется ареолярная грыжа, проявляющаяся выступающим сосково-ареолярным комплексом.
Субъективных симптомов (болей, дискомфорта) при тубулярности обычно не отмечается. В период кормления могут возникать затруднения из-за недостаточного образования молока по причине уменьшенного объема железистой ткани. При нарушении строения сосково-ареолярного комплекса ребенок не может правильно захватить грудь, что ведет к заглатыванию воздуха и дополнительно снижает количество молока.
Осложнения
При отсутствии лечения органические осложнения тубулярной груди не возникают. Имеются отдельные указания на более высокий риск развития мастопатий и связанных с ними нарушений, однако четкой корреляции не выявлено. Пациентки нередко страдают от психологических расстройств – эстетический дефект может стать причиной появления комплексов и развития неврозов. После хирургической коррекции порока иногда формируются гематомы, образуются грубые рубцы, возможно инфицирование операционной раны.
После хирургической коррекции порока иногда формируются гематомы, образуются грубые рубцы, возможно инфицирование операционной раны.
Диагностика
Постановка диагноза не представляет затруднений, осуществляется на основании результатов осмотра маммолога. Специалист определяет размеры и форму молочных желез, выявляет нарушение структуры органа (наличие уплотнений). Дифференциальную диагностику проводят с некоторыми типами мастопатий, особенно при асимметричной груди. Пальпаторное обнаружение уплотнений в структуре желез, втянутость сосков и наличие ареолярной грыжи являются поводом для назначения УЗИ груди и маммографии. Перечисленные исследования также проводятся в период подготовки к операции.
Коррекция тубулярной груди
Для устранения патологии используют хирургические методы лечения, их характер зависит от выраженности патологического состояния и пожеланий пациентки. Проводить операцию допустимо только при полностью сформированных молочных железах после достижения 22-24 лет. Ранняя коррекция может привести к появлению деформаций и изменению формы груди, для устранения которых потребуются дополнительные вмешательства. В тяжелых случаях (третий тип тубулярной груди) для восстановления эстетичного вида необходимо комплексное хирургическое лечение, общая продолжительность которого может составлять около 1 года.
Ранняя коррекция может привести к появлению деформаций и изменению формы груди, для устранения которых потребуются дополнительные вмешательства. В тяжелых случаях (третий тип тубулярной груди) для восстановления эстетичного вида необходимо комплексное хирургическое лечение, общая продолжительность которого может составлять около 1 года.
- Эндопротезирование груди. Для коррекции тубулярности пластические хирурги используют специальную технику установки имплантатов посредством периареолярного доступа. Для равномерного распределения паренхимы железы на ее ткань наносят насечки. В некоторых случаях требуется подбор специальных имплантатов для формирования симметричной груди.
- Установка тканевого эспандера. Применяется при втором и третьем типах состояния в рамках подготовки к эндопротезированию. Целью вмешательства является растяжение тканей для формирования ложа имплантата. После установки эспандера его наполняют изотоническим раствором, каждые две недели увеличивая объем.
 Длительность растяжения составляет не менее 2-3 месяцев в зависимости от выраженности недостатка тканей.
Длительность растяжения составляет не менее 2-3 месяцев в зависимости от выраженности недостатка тканей. - Уменьшение соска и ареолы. Операция может проводиться изолированно (при первом типе тубулярности) или как завершающий этап коррекции в случае более выраженной аномалии. Края ареолы иссекают, оставляя круг диаметром не более 4 сантиметров, и подшивают к коже.
Прогноз
Прогноз для жизни и здоровья при тубулярной груди благоприятный. Иногда отмечаются сложности с грудным вскармливанием, но в большинстве случаев жалобы пациенток связаны с неэстетичным видом груди и вторичными психологическими нарушениями. При коррекции возможны хирургические осложнения (гематомы, келоидные и гипертрофические рубцы, серома), однако их частота сравнительно невелика. В отдаленном периоде после операций может наблюдаться развитие контурирования или смещение имплантата, повреждение его оболочки.
Тубулярная грудь — причины, симптомы, диагностика и лечение
Тубулярная грудь – аномалия развития молочных желез, при которой уменьшается площадь их основания, возникает недостаток тканей, альвеолярная грыжа и птоз.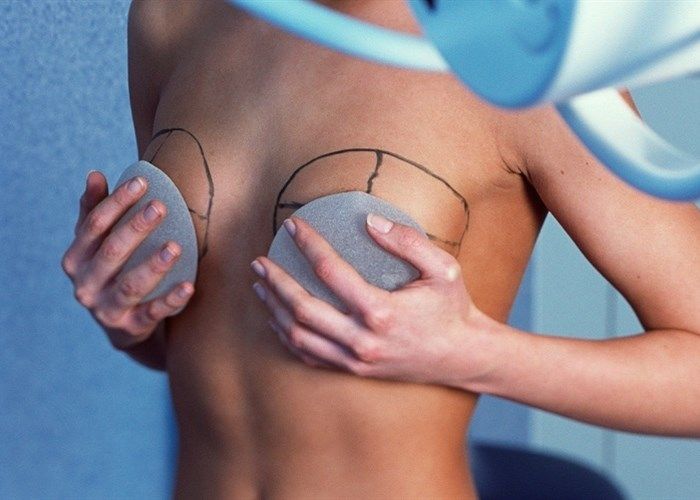 В результате вышеперечисленных нарушений грудь приобретает вытянутую «трубчатую» форму и неэстетичный внешний вид. Обычно патология выявляется с двух сторон, реже встречается поражение одной железы. Диагностика производится на основании данных осмотра, в качестве дополнительных методов в рамках предоперационной подготовки используют маммографию. Для коррекции применяют реконструктивные пластические операции с установкой эндопротезов (имплантатов).
В результате вышеперечисленных нарушений грудь приобретает вытянутую «трубчатую» форму и неэстетичный внешний вид. Обычно патология выявляется с двух сторон, реже встречается поражение одной железы. Диагностика производится на основании данных осмотра, в качестве дополнительных методов в рамках предоперационной подготовки используют маммографию. Для коррекции применяют реконструктивные пластические операции с установкой эндопротезов (имплантатов).
Общие сведения
Тубулярная грудь («козья грудь») происходит от латинского слова «tuba» – труба, поскольку вытянутая форма молочных желез на узком основании и с выпирающей ареолой похожа на трубку или цилиндр. Точные данные о распространенности отсутствуют, считается, что состояние выявляется примерно у 20 женщин из тысячи. Сложность определения встречаемости патологии обусловлена относительно редким обращением пациенток за медицинской помощью из-за отсутствия выраженной симптоматики (за исключением эстетического недостатка). Имеется расовая предрасположенность – у лиц негроидной расы подобная аномалия молочных желез регистрируется в несколько раз чаще.
Имеется расовая предрасположенность – у лиц негроидной расы подобная аномалия молочных желез регистрируется в несколько раз чаще.
Тубулярная грудь
Причины
Непосредственные причины развития данной патологии не установлены. По невыясненным обстоятельствам в тканях молочных желез возникают плотные соединительнотканные перемычки, которые формируют плотную сеть или футляр у основания органов. В процессе полового созревания перемычки растут медленнее, чем жировая и железистая ткань, деформируют железы, изменяют направление их роста в сторону ареолы и соска. С наружной стороны от футляра или сети жировая ткань не растет, что создает визуальную картину дефицита. Существует несколько теорий возникновения заболевания:
- Генетические факторы. Описаны семейные случаи развития тубулярной груди, наследование предположительно происходило по женской линии. Не выявлены ключевые гены, ответственные за развитие патологии, точный характер наследования и другие детали.

- Тератогенные факторы. Согласно этой гипотезе, аномалия имеет врожденный характер, обусловлена химическими или биологическими воздействиями на внутриутробном этапе развития.
- Приобретенные факторы. Некоторые исследователи отрицают врожденный характер как минимум части случаев порока развития, аргументируя это отсутствием изменений до начала подросткового периода. По их мнению, патология возникает из-за нарушения кровоснабжения тканей молочных желез, обусловленного заболеваниями, ношением неподходящих бюстгальтеров и пр.
Отсутствие точных данных относительно причин аномалии не позволяет заблаговременно выявлять заболевание и производить этиотропное лечение. Существующие гипотезы не объясняют ряд особенностей патогенеза данного состояния, поэтому его изучение продолжается.
Патогенез
Развитие тубулярной груди начинается в период полового созревания с началом роста молочных желез под влиянием женских половых гормонов и завершается к 17-20 годам. После этого аномалия прогрессирует крайне редко, беременность и кормление грудью лишь незначительно изменяют выраженность нарушения. Некоторые участки соединительнотканной стромы утолщаются и теряют эластичность, формируя плотное кольцо у основания железы. По мере роста девочки из соединительной ткани образуется плотный каркас или футляр, не позволяющий железистым и жировым структурам разрастаться в ширину.
После этого аномалия прогрессирует крайне редко, беременность и кормление грудью лишь незначительно изменяют выраженность нарушения. Некоторые участки соединительнотканной стромы утолщаются и теряют эластичность, формируя плотное кольцо у основания железы. По мере роста девочки из соединительной ткани образуется плотный каркас или футляр, не позволяющий железистым и жировым структурам разрастаться в ширину.
Рост нормальных железистых компонентов возможен только в пределах футляра, поэтому внешне нарушение проявляется как дефицит тканей на внутренней и нижней частях груди или по всей ее поверхности. В тяжелых случаях в процессе роста возникает сдавление тканей, ухудшается кровоснабжение молочных желез, что усиливает процессы склерозирования. У пациенток расширяется область ареолы, развивается состояние, известное как «ареолярная грыжа». В период лактации возможны трудности с кормлением ребенка, обусловленные нарушением питания железистой ткани, аномальной формой и размерами ареолы и соска.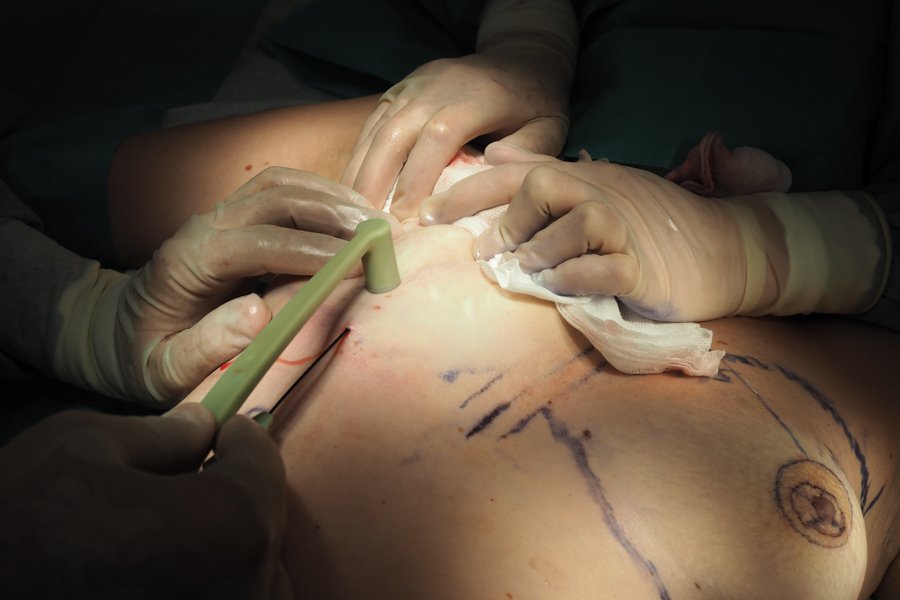
Классификация
В пластической хирургии выделяют три клинических формы тубулярной груди, отличающиеся степенью выраженности порока и, следовательно, недостатка тканей желез. Эти формы не являются последовательными стадиями аномалии развития.
- Первый тип. Из-за соединительнотканных перемычек затрудняется рост груди в медиальных и нижних квадрантах с возникновением дефицита тканей. Дефект выражен слабо, молочная железа несколько приподнята вверх, ареола и сосок не изменены. Патология часто не требует коррекции.
- Второй тип. Значительный недостаток тканей наблюдается в нижних квадрантах. Железа смещается вниз, при осмотре регистрируется расширение ареолы и уплощение соска.
- Третий тип. Формируется соединительнотканный футляр, который сужает основание желез и сильно препятствует их росту. Возникает существенный дефицит тканей. Рост тубулярной груди возможен только по направлению к соску, это приводит к резкому расширению сосково-ареолярного комплекса и развитию ареолярной грыжи.
Симптомы
Тубулярная грудь выявляется при внешнем осмотре. Молочные железы в зависимости от типа аномалии имеют конусовидную или цилиндрообразную форму. Основание органа сужено, что приводит к увеличению межгрудного пространства и птозу желез. Ареолы расширены, часто отмечается их недоразвитость (несоответствие возрасту женщины). Сосок уплощен, может наблюдаться его втягивание и разнообразные аномалии строения. В тяжелых случаях образуется ареолярная грыжа, проявляющаяся выступающим сосково-ареолярным комплексом.
Субъективных симптомов (болей, дискомфорта) при тубулярности обычно не отмечается. В период кормления могут возникать затруднения из-за недостаточного образования молока по причине уменьшенного объема железистой ткани. При нарушении строения сосково-ареолярного комплекса ребенок не может правильно захватить грудь, что ведет к заглатыванию воздуха и дополнительно снижает количество молока.
Осложнения
При отсутствии лечения органические осложнения тубулярной груди не возникают. Имеются отдельные указания на более высокий риск развития мастопатий и связанных с ними нарушений, однако четкой корреляции не выявлено. Пациентки нередко страдают от психологических расстройств – эстетический дефект может стать причиной появления комплексов и развития неврозов. После хирургической коррекции порока иногда формируются гематомы, образуются грубые рубцы, возможно инфицирование операционной раны.
Диагностика
Постановка диагноза не представляет затруднений, осуществляется на основании результатов осмотра маммолога. Специалист определяет размеры и форму молочных желез, выявляет нарушение структуры органа (наличие уплотнений). Дифференциальную диагностику проводят с некоторыми типами мастопатий, особенно при асимметричной груди. Пальпаторное обнаружение уплотнений в структуре желез, втянутость сосков и наличие ареолярной грыжи являются поводом для назначения УЗИ груди и маммографии. Перечисленные исследования также проводятся в период подготовки к операции.
Коррекция тубулярной груди
Для устранения патологии используют хирургические методы лечения, их характер зависит от выраженности патологического состояния и пожеланий пациентки. Проводить операцию допустимо только при полностью сформированных молочных железах после достижения 22-24 лет. Ранняя коррекция может привести к появлению деформаций и изменению формы груди, для устранения которых потребуются дополнительные вмешательства. В тяжелых случаях (третий тип тубулярной груди) для восстановления эстетичного вида необходимо комплексное хирургическое лечение, общая продолжительность которого может составлять около 1 года.
- Эндопротезирование груди. Для коррекции тубулярности пластические хирурги используют специальную технику установки имплантатов посредством периареолярного доступа. Для равномерного распределения паренхимы железы на ее ткань наносят насечки. В некоторых случаях требуется подбор специальных имплантатов для формирования симметричной груди.
- Установка тканевого эспандера. Применяется при втором и третьем типах состояния в рамках подготовки к эндопротезированию. Целью вмешательства является растяжение тканей для формирования ложа имплантата. После установки эспандера его наполняют изотоническим раствором, каждые две недели увеличивая объем. Длительность растяжения составляет не менее 2-3 месяцев в зависимости от выраженности недостатка тканей.
- Уменьшение соска и ареолы. Операция может проводиться изолированно (при первом типе тубулярности) или как завершающий этап коррекции в случае более выраженной аномалии. Края ареолы иссекают, оставляя круг диаметром не более 4 сантиметров, и подшивают к коже.
Прогноз
Прогноз для жизни и здоровья при тубулярной груди благоприятный. Иногда отмечаются сложности с грудным вскармливанием, но в большинстве случаев жалобы пациенток связаны с неэстетичным видом груди и вторичными психологическими нарушениями. При коррекции возможны хирургические осложнения (гематомы, келоидные и гипертрофические рубцы, серома), однако их частота сравнительно невелика. В отдаленном периоде после операций может наблюдаться развитие контурирования или смещение имплантата, повреждение его оболочки.
Тубулярная грудь — причины, симптомы, диагностика и лечение
Тубулярная грудь – аномалия развития молочных желез, при которой уменьшается площадь их основания, возникает недостаток тканей, альвеолярная грыжа и птоз. В результате вышеперечисленных нарушений грудь приобретает вытянутую «трубчатую» форму и неэстетичный внешний вид. Обычно патология выявляется с двух сторон, реже встречается поражение одной железы. Диагностика производится на основании данных осмотра, в качестве дополнительных методов в рамках предоперационной подготовки используют маммографию. Для коррекции применяют реконструктивные пластические операции с установкой эндопротезов (имплантатов).
Общие сведения
Тубулярная грудь («козья грудь») происходит от латинского слова «tuba» – труба, поскольку вытянутая форма молочных желез на узком основании и с выпирающей ареолой похожа на трубку или цилиндр. Точные данные о распространенности отсутствуют, считается, что состояние выявляется примерно у 20 женщин из тысячи. Сложность определения встречаемости патологии обусловлена относительно редким обращением пациенток за медицинской помощью из-за отсутствия выраженной симптоматики (за исключением эстетического недостатка). Имеется расовая предрасположенность – у лиц негроидной расы подобная аномалия молочных желез регистрируется в несколько раз чаще.
Тубулярная грудь
Причины
Непосредственные причины развития данной патологии не установлены. По невыясненным обстоятельствам в тканях молочных желез возникают плотные соединительнотканные перемычки, которые формируют плотную сеть или футляр у основания органов. В процессе полового созревания перемычки растут медленнее, чем жировая и железистая ткань, деформируют железы, изменяют направление их роста в сторону ареолы и соска. С наружной стороны от футляра или сети жировая ткань не растет, что создает визуальную картину дефицита. Существует несколько теорий возникновения заболевания:
- Генетические факторы. Описаны семейные случаи развития тубулярной груди, наследование предположительно происходило по женской линии. Не выявлены ключевые гены, ответственные за развитие патологии, точный характер наследования и другие детали.
- Тератогенные факторы. Согласно этой гипотезе, аномалия имеет врожденный характер, обусловлена химическими или биологическими воздействиями на внутриутробном этапе развития.
- Приобретенные факторы. Некоторые исследователи отрицают врожденный характер как минимум части случаев порока развития, аргументируя это отсутствием изменений до начала подросткового периода. По их мнению, патология возникает из-за нарушения кровоснабжения тканей молочных желез, обусловленного заболеваниями, ношением неподходящих бюстгальтеров и пр.
Отсутствие точных данных относительно причин аномалии не позволяет заблаговременно выявлять заболевание и производить этиотропное лечение. Существующие гипотезы не объясняют ряд особенностей патогенеза данного состояния, поэтому его изучение продолжается.
Патогенез
Развитие тубулярной груди начинается в период полового созревания с началом роста молочных желез под влиянием женских половых гормонов и завершается к 17-20 годам. После этого аномалия прогрессирует крайне редко, беременность и кормление грудью лишь незначительно изменяют выраженность нарушения. Некоторые участки соединительнотканной стромы утолщаются и теряют эластичность, формируя плотное кольцо у основания железы. По мере роста девочки из соединительной ткани образуется плотный каркас или футляр, не позволяющий железистым и жировым структурам разрастаться в ширину.
Рост нормальных железистых компонентов возможен только в пределах футляра, поэтому внешне нарушение проявляется как дефицит тканей на внутренней и нижней частях груди или по всей ее поверхности. В тяжелых случаях в процессе роста возникает сдавление тканей, ухудшается кровоснабжение молочных желез, что усиливает процессы склерозирования. У пациенток расширяется область ареолы, развивается состояние, известное как «ареолярная грыжа». В период лактации возможны трудности с кормлением ребенка, обусловленные нарушением питания железистой ткани, аномальной формой и размерами ареолы и соска.
Классификация
В пластической хирургии выделяют три клинических формы тубулярной груди, отличающиеся степенью выраженности порока и, следовательно, недостатка тканей желез. Эти формы не являются последовательными стадиями аномалии развития.
- Первый тип. Из-за соединительнотканных перемычек затрудняется рост груди в медиальных и нижних квадрантах с возникновением дефицита тканей. Дефект выражен слабо, молочная железа несколько приподнята вверх, ареола и сосок не изменены. Патология часто не требует коррекции.
- Второй тип. Значительный недостаток тканей наблюдается в нижних квадрантах. Железа смещается вниз, при осмотре регистрируется расширение ареолы и уплощение соска.
- Третий тип. Формируется соединительнотканный футляр, который сужает основание желез и сильно препятствует их росту. Возникает существенный дефицит тканей. Рост тубулярной груди возможен только по направлению к соску, это приводит к резкому расширению сосково-ареолярного комплекса и развитию ареолярной грыжи.
Симптомы
Тубулярная грудь выявляется при внешнем осмотре. Молочные железы в зависимости от типа аномалии имеют конусовидную или цилиндрообразную форму. Основание органа сужено, что приводит к увеличению межгрудного пространства и птозу желез. Ареолы расширены, часто отмечается их недоразвитость (несоответствие возрасту женщины). Сосок уплощен, может наблюдаться его втягивание и разнообразные аномалии строения. В тяжелых случаях образуется ареолярная грыжа, проявляющаяся выступающим сосково-ареолярным комплексом.
Субъективных симптомов (болей, дискомфорта) при тубулярности обычно не отмечается. В период кормления могут возникать затруднения из-за недостаточного образования молока по причине уменьшенного объема железистой ткани. При нарушении строения сосково-ареолярного комплекса ребенок не может правильно захватить грудь, что ведет к заглатыванию воздуха и дополнительно снижает количество молока.
Осложнения
При отсутствии лечения органические осложнения тубулярной груди не возникают. Имеются отдельные указания на более высокий риск развития мастопатий и связанных с ними нарушений, однако четкой корреляции не выявлено. Пациентки нередко страдают от психологических расстройств – эстетический дефект может стать причиной появления комплексов и развития неврозов. После хирургической коррекции порока иногда формируются гематомы, образуются грубые рубцы, возможно инфицирование операционной раны.
Диагностика
Постановка диагноза не представляет затруднений, осуществляется на основании результатов осмотра маммолога. Специалист определяет размеры и форму молочных желез, выявляет нарушение структуры органа (наличие уплотнений). Дифференциальную диагностику проводят с некоторыми типами мастопатий, особенно при асимметричной груди. Пальпаторное обнаружение уплотнений в структуре желез, втянутость сосков и наличие ареолярной грыжи являются поводом для назначения УЗИ груди и маммографии. Перечисленные исследования также проводятся в период подготовки к операции.
Коррекция тубулярной груди
Для устранения патологии используют хирургические методы лечения, их характер зависит от выраженности патологического состояния и пожеланий пациентки. Проводить операцию допустимо только при полностью сформированных молочных железах после достижения 22-24 лет. Ранняя коррекция может привести к появлению деформаций и изменению формы груди, для устранения которых потребуются дополнительные вмешательства. В тяжелых случаях (третий тип тубулярной груди) для восстановления эстетичного вида необходимо комплексное хирургическое лечение, общая продолжительность которого может составлять около 1 года.
- Эндопротезирование груди. Для коррекции тубулярности пластические хирурги используют специальную технику установки имплантатов посредством периареолярного доступа. Для равномерного распределения паренхимы железы на ее ткань наносят насечки. В некоторых случаях требуется подбор специальных имплантатов для формирования симметричной груди.
- Установка тканевого эспандера. Применяется при втором и третьем типах состояния в рамках подготовки к эндопротезированию. Целью вмешательства является растяжение тканей для формирования ложа имплантата. После установки эспандера его наполняют изотоническим раствором, каждые две недели увеличивая объем. Длительность растяжения составляет не менее 2-3 месяцев в зависимости от выраженности недостатка тканей.
- Уменьшение соска и ареолы. Операция может проводиться изолированно (при первом типе тубулярности) или как завершающий этап коррекции в случае более выраженной аномалии. Края ареолы иссекают, оставляя круг диаметром не более 4 сантиметров, и подшивают к коже.
Прогноз
Прогноз для жизни и здоровья при тубулярной груди благоприятный. Иногда отмечаются сложности с грудным вскармливанием, но в большинстве случаев жалобы пациенток связаны с неэстетичным видом груди и вторичными психологическими нарушениями. При коррекции возможны хирургические осложнения (гематомы, келоидные и гипертрофические рубцы, серома), однако их частота сравнительно невелика. В отдаленном периоде после операций может наблюдаться развитие контурирования или смещение имплантата, повреждение его оболочки.
Коррекция тубулярной груди (операция маммопластика)
Тубулярность – врожденная патология развития молочных желез, характеризующаяся уменьшением диаметра их основания, дефицитом тканей, птозом и альвеолярной грыжей. Бюст в результате таких нарушений становится вытянутым (название заболевания происходит от лат. tuba – «труба»), принимает неэстетичный внешний вид. Чаще всего тубулярность – двухсторонняя, но встречаются деформации только одной молочной железы. Выявляется такая патология примерно у 2% женщин, в несколько раз чаще она диагностируется у представительниц негроидной расы.
Методы лечения тубулярной груди: операция маммопластика
Для коррекции тубулярных молочных желез применяются хирургические методики. Операция делается пациенткам в возрасте старше 22-23-х лет, потому что необходимое условие для вмешательства – завершение формирования бюста. Если пластику сделать слишком рано, то грудь продолжит меняться и деформироваться, и позднее нужно будет снова оперировать пациентку.
При тяжелых случаях патологии восстановление эстетичной формы может занять 1 год, оно будет включать различные хирургические методики.
- Протезирование – для коррекции тубулярной груди врачи применяют особую технику увеличения специальными имплантатами. Доступ в этом случае – периареолярный. Чтобы равномерно распределить железу по эндопротезу, на ней делают насечки.
- Установка эспандера. Это необходимая мера при II и III типах патологии. Это начальный этап коррекции тубулярной молочной железы, подготовка к протезированию груди. Эспандер работает на растяжение тканей при их дефиците. Каждые 2 недели его все больше наполняют специальным раствором, увеличивая понемногу его объем. За счет этого ткани растягиваются и появляется возможность установить имплантат. Срок растяжения колеблется, в зависимости от того, насколько велик дефицит тканей, но как минимум эспандер носят 2-3 месяца.
- Коррекция сосково-ареолярного комплекса. При I типе тубулярной груди эта пластика может проводиться отдельно, то есть если женщина имеет дефект только в этой области. При более выраженной тубулярности такое вмешательство – завершающий этап коррекции бюста. Пластический хирург иссекает края ареолы, чтобы она приобрела диаметр не более 4-х см, а затем подшивает ее к коже груди.
В общем виде операция пошагово выглядит так:
- Обеспечение общей анестезии, обеззараживание области вмешательства.
- Два разреза в зоне ареолы.
- Формирование ложа для эндопротеза. Подготовка к установке имплантата.
- Установка эндопротеза и дренажной трубки.
- Формирование сосково-ареолярного комплекса.
- Наложение швов.
Возможные сложности при проведении пластики тубулярной деформации молочной железы
Эта операция считается достаточно сложной и требует от хирурга высокого мастерства и опыта.
Если только лишь увеличивать бюст, не применяя других методик, возможно осложнение, называемое хирургами «dubble bubble», это двойная складка под грудью. Для предотвращения ее появления форму желез меняют, делая надрезы и тщательно расправляя ткани на эндопротезе. Когда железистых тканей не хватает для покрытия имплантата, объем восполняют по методу липофилинга – добавляют в места дефицита собственный жир пациентки, взятый из зоны живота, ягодиц или бедер.
Трудно поддаются коррекции аномалии, сопровождающиеся остаточной асимметрией, дефицитом мягких тканей, которыми нужно покрыть нижнюю часть эндопротеза, уплощенностью груди в нижней части.
Акция
Увеличение груди по программе «Все включено»
Срок действия акции: до 31 марта 2021 года
Ваша выгода: 8 %
Стоимость операции: 180 000 руб
Записаться к врачуПодробнее об акции
Результаты маммопластики
Эффект пациентка может оценить примерно через 6 месяцев, когда закончат формироваться новые очертания груди, установится симметрия, полностью спадет отек. Операция по коррекции сложная, период восстановления долгий, но результат неизменно радует – хирурги достигают максимально естественного внешнего вида бюста без видимых следов вмешательства. Грудь становится анатомически правильной, красивой, ареолы – аккуратными и ровными.
Женщины, планирующие рождение детей, могут не опасаться ограничений – возможность грудного кормления сохраняется.
Нестандартное строение груди объясняется аномалией развития. Тубулярная грудь располагается не в плоскости грудной мышцы, а выступает вперед в трубчатом виде. Тубулярной груди, кроме того, свойственна периареолярная грыжа и растянутость ареолы.
Калита Екатерина Романовна
Постоянный участник конференций и семинаров по пластической хирургии. Приоритетные направления: пластика груди, абдоминопластика, интимная пластика, комбинированная омолаживающая пластика лица, отопластика у детей и взрослых, блефаропластика. Аспирант кафедры Термических поражений и пластической хирургии Военно-Медицинской академии.
Опущение груди: лечение птоза грудных желез
Для большинства женщин опущение груди — серьезная эстетическая проблема, которая мешает полюбить собственное тело и вызывает комплексы, поэтому вопрос о лечении птоза грудных желез стоит особенно актуально. Инволюционные процессы старения, генетическая предрасположенность и ежеминутное воздействие гравитационных сил Земли способствуют естественному птозу кожи, тканей организма и некоторых внутренних органов. Если речь идет об опущении молочных желез, то в медицине его называют «мастоптозом». При мастоптозе грудь женщины теряет упругую форму и выглядит обвисшей. Специальный уход в профилактических целях помогает лишь замедлить процесс опущения груди. К нему относятся: контрастный душ, массажи, обертывания, косметические средства, мезотерапия, биоревитализация кожи груди, а также некоторые другие салонные процедуры. Однако при выраженном мастоптозе консервативные методы уже неэффективны. В этой статье мы расскажем о возможных способах лечения птоза грудных желез. Самым быстрым и эффективным из них по-прежнему остается мастопексия (маммопексия) — пластическая операция по подтяжке молочных желез с применением имплантов или без них. Но сначала разберем, почему же вообще обвисает грудь: какие факторы этому способствуют?
Причины птоза молочных желез
Объем и внешний вид женского бюста определяют: состояние большой грудной мышцы и связок, соотношение жировой и железистой ткани, сформированной в дольки.
- Возрастные изменения — со временем, примерно после 45 лет, в организме женщины запускается процесс фиброзно-жировой инволюции молочных желез. Он заключается в деградации железистой ткани и ее постепенном замещении тканью жировой. Это происходит на фоне гормональных изменений, которые особенно активно осуществляются в период менопаузы. Эти изменения приводят к дефициту половых гормонов эстрогенов и постепенному «угасанию» организма. Замедляется синтез коллагена и эластана, которые являются структурными компонентами соединительной ткани, дермы и связок. В результате фиброзно-жировой инволюции грудь женщины теряет эстетически привлекательный вид и под воздействием естественных гравитационных сил Земли опускается.
- Наследственный фактор — врожденные особенности синтеза коллагена и эластина определяют скорость старения тканей и предрасположенность к гигантомастии, а следовательно, и к мастоптозу.
- Беременность и грудное вскармливание — во время беременности грудь женщины увеличивается в объеме за счет наполнения железистых долек молоком. При этом возрастает нагрузка на связки, а кожа растягивается. После завершения лактации объем железы постепенно уменьшается. Из-за растяжения кожи грудь выглядит «пустой» и обвисшей. Кроме того, неравномерное распределение молока, а также кормление ребенка одной грудью, может привести к заметной асимметрии.
- Стремительное похудение или набор веса — жировая клетчатка не только фактически определяет форму молочных желез. В случае быстрого похудения теряется часть объема груди, а кожа не успевает восстановиться. В адипоцитах жировой ткани хранятся и синтезируются гормоны, которые отвечают за обмен веществ. Напротив, стремительный набор веса приводит к увеличению объема молочных желез и растяжению кожи.
- Эндопротезирование молочных желез слишком большими имплантами — опущение груди после маммопластики происходит тем быстрее, чем больше протез и чем менее эластична кожа.
- Курение и злоупотребление алкоголем.
Стадии мастоптоза
Согласно классификации, предложенной американскими пластическими хирургами, существует 3 степени мастоптоза.
Птоз груди 1 степени — начальная стадия опущения груди, при которой сосок находится на уровне субмаммарной (подгрудной) складки или чуть ниже.
Птоз груди 2 степени — сосок опускается менее чем на 3 см ниже субмаммарной складки.
Птоз груди 3 степени — сосок расположен более чем на 3 см ниже уровня складки и смотрит вниз.
Ложный птоз (мастоптоз) характеризуется нормальным положением сосков и провисанием нижнего полюса молочных желез — он находится под субмаммарной складкой.
Лечение птоза груди
С помощью физических упражнений и диеты можно уменьшить объем жировой клетчатки, однако на состоянии соединительной и железистой ткани, которые также придают форму груди это не отражается. К тому же, при мастоптозе проблема заключается также и в растяжении кожи.
Напротив, лифтинг груди в салоне (мезотерапия, биоревитализация, массаж и другие косметологические процедуры) направлен на улучшение состояния соединительной ткани. Эти безоперационные методы требуют регулярного повторения и они не исправят выраженный птоз груди. Инъекции витаминных комплексов, гиалуроновый кислоты и других активных веществ помогут добиться качественного улучшения состояния кожи, восстановления синтеза волокон коллагена и эластана. Благодаря косметологическим процедурам можно замедлить процессы старения и улучшить внешний вид груди, но не исправить птоз груди или ее форму.
Как исправить птоз с помощью хирургической подтяжки (мастопексии)
При птозе груди 1 степени вернуть бюсту красивую форму можно с помощью эндопротезирования — операции по его увеличению имплантами. Проблема более запущенного птоза 2 или 3 степени решается мастопексией (маммопексией), то есть подтяжкой груди. Суть этой пластической операции заключается в резекции избыточной кожи, жировой и железистой ткани, в результате чего удается приподнять сосково-ареолярный комплекс. При недостаточном объеме тканей молочной железы мастопексию можно совместить с эндопротезированием и таким образом увеличить размер груди. Если у женщины наблюдается заметная асимметрия, то устранить ее можно путем сочетания подтяжки с редукционной маммопластикой или эндопротезированием. В целом, мастопексия выполняется под общей анестезией в течение 1-3 часов.
Существует три основных метода подтяжки груди:
Периареолярная мастопексия
Применяется для устранения легкого и неосложненного птоза 1 или 2 степени. Пластический хирург делает разрез вокруг ареолы, чтобы выполнить резекцию излишков кожи.
Вертикальная мастопексия
Метод используется при птозе груди 2 и 3 степени. Пластический хирург делает два разреза: один вокруг ареолы, а другой — вертикально вниз от окружности на 7-8 см.
Якорная (или «Т-образная») мастопексия
Самый эффективный способ устранения запущенного птоза груди 3 степени. Методика предполагает композицию из трех аккуратных разрезов: вертикального, вокруг ареолы и по контуру субмаммарной складки.
Почему подтяжку груди стоит сделать в клинике им. Н.И. Пирогова?
Наши пластические хирурги знают, как исправить птоз груди, придав ей снова красивую и подтянутую форму без заметных послеоперационных рубцов. Посмотрите портфолио наших специалистов, и вы сможете в этом убедиться. С 1999 года врачи клиники им. Н.И. Пирогова в Санкт-Петербурге успешно выполняют все виды операций на молочной железе: от эндопротезирования до реконструкции после мастэктомии. Если спустя некоторое время вы столкнулись с проблемой опущения груди после первичной маммопластики, наши пластические хирурги не только решат эту проблему, но позаботятся о качественном и продолжительном сохранении результата. Мы предлагаем нашим пациентам:
- услуги ведущих в городе пластических хирургов;
- медицинские кабинеты, оснащенные современным оборудованием на уровне европейских частных клиник;
- пребывание в палатах на 1-2 человек повышенной комфортности с питанием, уходом медицинских сестер и круглосуточным наблюдением дежурного врача;
- специальные акционные предложения (все включено) по демократичным ценам;
- собственную лабораторию, которая позволяет быстро получить точные результаты диагностики, и реанимацию;
- услуги отделения косметологии, которые могут быть полезны для профилактики и лечения птоза груди в легкой форме;
- организационную помощь куратора для пациентов из других городов.
ЭФФЕКТИВНОСТЬ ПРОВЕТРИВАНИЯ ТУПИКОВЫХ ПОДГОТОВИТЕЛЬНЫХ ВЫРАБОТОК ПОСЛЕ ВЗРЫВНЫХ РАБОТ
Актуальность исследования обусловлена необходимостью улучшениясистемы вентиляции тупиковых выработок, сокращения трудозатрат на ихвентиляцию и ускорения выполнения основных операций по проходке выработок. Цель: определение оптимального расстояния от конца трубопровода до груди забоя тупиковой выработки с точки зрения эффективности проветривания тупиковой подготовительной выработки. Объект: система вентиляции тупиковой подготовительной выработки. Методы:многопараметрическоетрехмерное численное моделирование на основе методов вычислительной гидродинамики. Приведены результаты трехмерного численного моделирования проветривания тупиковой подготовительной выработки от выделившихся в результате взрывных работ ядовитых газов. Варьируемыми параметрами модели являются: начальная концентрация и распределение вредных примесей в тупиковой выработке после проведения взрывных работ, расстояние от конца нагнетательного трубопровода до тупикового забоя, поперечное сечение тупиковой выработки, а также расход свежего воздуха, поступающего через трубопровод. Получена расчетная формула для определения объема зоны смешения.Показано, что время проветривания тупиковой выработки не зависит от длины зоны отброса газов, а зависит от начальной средней концентрации ядовитых газов в зоне смешения.Получены значения безразмерного коэффициента эффективности проветривания Kтупиковой выработки, или коэффициента турбулентной диффузии В.Н. Воронина, в зависимости от варьируемых параметров. Показано, что коэффициент K не зависит от величины входящего расхода свежего воздуха, а зависит только от геометрических параметров системы вентиляции тупиковой выработки и принимает постоянное значение для данной конфигурации системы вентиляции.Показано, что существует оптимальное расстояние от конца трубопровода до забоя, при котором происходит наиболее эффективный вынос вредных примесей.
Шумовое полев грудной клетке человека из-за турбулентного потока в большом кровеносном сосуде
Гидденс, Д.П., Мабон, Р.Ф. и Кассанова, Р.А., Измерение неупорядоченного кровотока от дистального к субтотальному стенозу сосудов в грудной аорте собак. Circ. Res. 39 (1976) 112–119.
Google Scholar
Тобин, Р.Дж. и Чанг, И.Д. Масштабирование спектров давления на стенке за стенозами при установившемся потоке через трубку. J. Biomech. 9 (1976) 633–640.
Артикул Google Scholar
Кларк, К., Измерения турбулентной скорости в модели стеноза аорты. J. Biomech. 9 (1976) 677–687.
Артикул Google Scholar
Кларк, К., Измерение турбулентного давления стенки в модели стеноза аорты. J. Biomech. 10 (1977) 461–472.
Артикул Google Scholar
Халифа А.М. и Гидденс, Д.П., Анализ беспорядка пульсирующих потоков в приложении к измерению скорости кровотока после стеноза у собак. J. Biomech. 11 (1978) 129–141.
Артикул Google Scholar
Gosling, R.G. и King, D.H., Ультразвук непрерывной волны как альтернатива и дополнение к рентгеновским лучам при обследовании сосудов. В: Ренеман, Р. (ред.), Сердечно-сосудистые применения ультразвука . Эльзевир, Нью-Йорк (1974), стр. 266–282.
Google Scholar
Fitzgerald, D.E. и Карр Дж. Ультразвуковая допплерография и классификация как альтернатива артериографии. Ангиология 26 (1975) 283–288.
Google Scholar
Lees, R.S. и Дьюи, К.Ф., младший, Фоноангиография: новый неинвазивный диагностический метод для изучения артериальных заболеваний. Proc. Nat. Акад. Sci. 67 (1970) 935–942.
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Фредберг Дж. Дж. Генерация псевдозвука при атеросклеротических сужениях артерий. Бык. Математика. Биол. 36 (1974) 143–155.
МАТЕМАТИКА Статья Google Scholar
Фредберг, Дж. Дж., Происхождение и характер сосудистых шумов: модельные исследования. J. Acoust. Soc. Амер. 61 (1977) 1077–1085.
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Дункан, Г.W., Gruber, J.O., Dewey, C.F., Jr., Myers, G.S. и Lees, R.S., Оценка стеноза сонной артерии с помощью фоноангиографии. Новый англ. J. Med. 293 (1975) 1124–1128.
Артикул Google Scholar
Питтс, У.Х., III и Дьюи, К.Ф., мл., Спектральные и временные характеристики постстенотических турбулентных колебаний давления на стенке. ASME J. Biomech. Engrg. 101 (1979) 89–95.
Google Scholar
Гавриэли Н., Палто Ю. и Алрой Г. Спектральные характеристики нормальных звуков дыхания. J. Appl. Physiol. 50 (1980) 307–314.
Google Scholar
Краман С.С. Определение места производства респираторных звуков методом субтрактивной фонопневмографии. амер. Ред.Респ. Дис. 122 (1980) 303–314.
Google Scholar
Шарбонне, Г., Ракцине, Дж. Л., Субро, М. и Туше, Э., Точная система записи и ее использование в спектральном анализе дыхательных звуков. J. Appl. Physiol. 55 (1983) 1120–1127.
Google Scholar
Коэн, А.и Ландсберг Д. Анализ и автоматическая классификация звуков дыхания. IEEE + wans. Биомед. Engrg. БМЕ-31 (1984) 585–590.
Google Scholar
Вовк И.В., Гринченко В.Т., Красный Л.Г. , Макаренков А.П. Звуки дыхания: проблемы записи и классификации. Акуст. Журн. 40 (1994) 50–56.
Google Scholar
Макаренков А.П., Рудницкий А.Г. Диагностика патологий легких по двухканальной обработке звуков дыхания. Акуст. Журн. 41 (1995) 272–277.
Google Scholar
Борисюк А.О. Шумообразование потоком в трубах при наличии стеновых преград. Rep. Acad. Sci. Укр. 11 (1996) 66–70 [на украинском языке].
МАТЕМАТИКА Google Scholar
Борисюк А.А. Шум, создаваемый постоянным потоком в кровеносных сосудах человека при стенозах. Бионика 27-28 (1998) 144–151.
Google Scholar
Ким Б. и Коркоран В. К. Экспериментальное измерение спектров турбулентности дистальнее стеноза. Дж.Биомех. 7 (1974) 335–342.
Артикул Google Scholar
Ван Дж., Ти Б., Велковиц В., Семмлоу Дж. Л. и Костис Дж. Б. Моделирование генерации звука в стенозированных коронарных артериях. IEEE Trans. Биомед. Engrg. 37 (1990) 1087–1094.
Артикул Google Scholar
Водичка Г.Р., Стивенс К.Н., Голуб Х.Л., Growalho E.G. и Шенон, Д.С., Модель передачи звука в дыхательной системе. IEEE Trans. Биомед. Engrg. 36 (1989) 925–933.
Артикул Google Scholar
Водичка Г.Р., Стивенс К.Н., Голуб Х.Л. и Шанон Д.С. Спектральные характеристики передачи звука в дыхательной системе человека. IEEE Trans.Биомед. Engrg. 37 (1990) 1130–1134.
Артикул Google Scholar
Вовк И.В., Залуцкий К.Е. А., Красный Л.Г. Акустическая модель дыхательной системы человека. Акуст. Журн. 40 (1994) 762–767.
Google Scholar
Коркос Г. М. Разрешение давления в условиях турбулентности. J. Acoust. Soc. Амер. 35 (1963) 192–199.
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Борисюк А.О. А., Гринченко В.Т. Генерация вибрации и шума упругим элементом, возбуждаемым турбулентным потоком. J. Sound Vibr. 204 (1997) 213–237.
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Мартин Н.К. и Лихи П. Измерения давления на стенке с низким волновым числом с использованием прямоугольной мембраны в качестве пространственного фильтра. J. Sound Vibr. 52 (1977) 95–120.
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Янг Д.Ф. Гидравлическая механика артериальных стенозов. J. Biomech. Engrg. 101 (1979) 157–175.
Google Scholar
Миролюбов С.Г. Гидродинамика стеноза. Модерн Пробл. Биомех. 1 (1983) 73–136.
Google Scholar
Blake, W.K. (ред.), Механика звука и вибрации, вызванного потоком (два тома). Academic Press, New York (1986) 954 стр.
MATH Google Scholar
Ффоукс Уильямс, Дж.Д., Давление в пограничном слое и модель Коркоса: разработка для включения ограничений с низким волновым числом. J. Fluid Mech. 125 (1982) 9–25.
МАТЕМАТИКА Статья ОБЪЯВЛЕНИЯ Google Scholar
Смольяков А.В. , Ткаченко В.М. Модели псевдозвукового турбулентного поля пристенного давления и экспериментальные данные. Акуст. Журн. 37 (1991) 1199–1207.
ADS Google Scholar
Чейз Д.М. Моделирование частотно-волнового спектра давления на стенке турбулентного пограничного слоя. J. Sound Vibr. 70 (1980) 29–67.
МАТЕМАТИКА Статья ОБЪЯВЛЕНИЯ Google Scholar
Шумы в сердце — симптомы и причины
Обзор
Шумы в сердце — это звуки, такие как свист или свист, производимые бурной кровью в сердце или рядом с ним.Ваш врач может услышать эти звуки с помощью стетоскопа. Нормальное сердцебиение издает два звука, похожие на «лаб-дупп» (иногда его называют «луб-дуп»), когда ваши сердечные клапаны закрываются.
Шумы в сердце могут присутствовать при рождении (врожденные) или развиваться в более позднем возрасте.
Шумы в сердце могут быть безвредными (невинными) или ненормальными. Невинный шум в сердце не является признаком болезни сердца и не требует лечения. Аномальные шумы в сердце требуют повторного обследования для определения причины. Лечение направлено на устранение причины аномального шума в сердце.
Симптомы
Если у вас невинный шум в сердце, у вас, скорее всего, не будет никаких других признаков или симптомов.
Аномальный шум в сердце может вызывать следующие признаки и симптомы, в зависимости от причины шума:
- Синяя кожа, особенно на кончиках пальцев и губ
- Отек или резкое увеличение веса
- Одышка
- Хронический кашель
- Увеличенная печень
- Расширенные шейные вены
- У младенцев плохой аппетит и нарушение нормального роста
- Сильное потоотделение с незначительной или нулевой активностью
- Боль в груди
- Головокружение
- Обморок
Когда обращаться к врачу
Большинство шумов в сердце несерьезны, но если вы считаете, что у вас или вашего ребенка шум в сердце, запишитесь на прием к семейному врачу.Ваш врач может сказать вам, является ли шум в сердце безобидным и не требует дальнейшего лечения, или требуется дополнительное обследование основной проблемы с сердцем.
Причины
Может возникнуть шум в сердце:
- Когда сердце наполняется кровью (диастолический шум)
- Когда сердце опорожняется (систолический шум)
- На протяжении всего сердцебиения (непрерывный шум)
Шум в сердце может быть невинным или ненормальным.
Невинный шум в сердце
У человека с невинным шумом сердце нормальное. Этот тип шума в сердце часто встречается у новорожденных и детей.
Невинный шум может возникнуть, когда кровь течет через сердце быстрее, чем обычно. Состояния, которые могут вызвать учащенный кровоток в сердце, приводящий к невинному шуму в сердце, включают:
- Физическая активность или упражнения
- Беременность
- Лихорадка
- Отсутствие достаточного количества здоровых эритроцитов для доставки кислорода к тканям тела (анемия)
- Слишком много гормона щитовидной железы в организме (гипертиреоз)
- Фазы быстрого роста, например подростковый возраст
Невинные шумы в сердце могут исчезнуть со временем или могут длиться всю жизнь, не вызывая дальнейших проблем со здоровьем.
Аномальные шумы в сердце
У взрослых аномальные шумы чаще всего возникают из-за приобретенных проблем с сердечным клапаном. У детей аномальные шумы обычно вызваны структурными проблемами сердца (врожденные пороки сердца).
Общие врожденные дефекты, вызывающие шумы в сердце, включают:
- Отверстия в сердце. Дыры в сердце, известные как дефекты перегородки, могут быть или не быть серьезными, в зависимости от размера отверстия и его местоположения.
- Сердечные шунты. Сердечные шунты возникают при аномальном кровотоке между камерами сердца или кровеносными сосудами, что может привести к шуму в сердце.
- Проблемы с сердечным клапаном присутствуют с рождения. Примеры включают клапаны, которые не пропускают через них достаточное количество крови (стеноз), или клапаны, которые не закрываются должным образом и вытекают (срыгивание).
У детей старшего возраста и взрослых причины аномальных шумов в сердце включают инфекции и состояния, повреждающие структуры сердца.Например:
- Кальцификация клапана. Это уплотнение или утолщение клапанов, как при митральном стенозе или стенозе аортального клапана, может происходить с возрастом. Клапаны могут сужаться (стенозироваться), затрудняя кровоток через сердце, что приводит к появлению шумов.
Эндокардит. Эта инфекция внутренней оболочки сердца и клапанов обычно возникает, когда бактерии или другие микробы из другой части вашего тела, например изо рта, распространяются через кровоток и застревают в вашем сердце.
При отсутствии лечения эндокардит может повредить или разрушить клапаны сердца. Это состояние обычно возникает у людей, у которых уже есть проблемы с сердечным клапаном.
- Ревматическая лихорадка. Ревматическая лихорадка, которая сейчас редко встречается в Соединенных Штатах, представляет собой серьезное заболевание, которое может возникнуть, если вы не получите немедленного или полного лечения от стрептококковой инфекции горла. Это может необратимо повлиять на сердечные клапаны и нарушить нормальный кровоток через сердце.
Факторы риска
У вас повышенный риск сердечного шума, если у кого-то из членов вашей семьи был порок сердца, связанный с необычными звуками.
Множество различных заболеваний могут увеличить риск возникновения сердечных шумов, в том числе:
- Ослабленная сердечная мышца (кардиомиопатия)
- Инфекция внутренней оболочки сердца (эндокардит)
- Заболевания крови, отмеченные большим количеством определенных белых клеток, называемых эозинофилами (гиперэозинофильный синдром)
- Некоторые аутоиммунные заболевания, включая волчанку и ревматоидный артрит
- Химические вещества из редкой опухоли легких или желудочно-кишечного тракта, попавшие в кровоток (карциноидный синдром)
- Порок клапана сердца
- Высокое артериальное давление (гипертония)
- Повышенное артериальное давление в легких (легочная гипертензия)
- История ревматической лихорадки
- Сверхактивная щитовидная железа (гипертиреоз)
Неконтролируемый диабет или инфекция краснухи во время беременности увеличивает риск развития порока сердца и шума в сердце у вашего ребенка.Использование определенных лекарств, алкоголя или наркотиков во время беременности может привести к порокам сердца у развивающегося ребенка, что может вызвать шум в сердце.
Профилактика
Хотя вы мало что можете сделать для предотвращения шума в сердце, приятно знать, что шум в сердце не является заболеванием и часто безвреден. У детей многие шепоты проходят сами по себе, когда дети растут. У взрослых шумы могут исчезнуть по мере улучшения основного состояния, вызвавшего их.
Опыт и истории пациентов клиники Мэйо
Наши пациенты говорят нам, что качество их общения, наше внимание к деталям и эффективность их посещений означают такое медицинское обслуживание, которого они никогда не получали. Посмотрите истории довольных пациентов клиники Мэйо.
Когда ему предстоит сложная операция на сердце, врач выбирает клинику Мэйо
Когда он узнал, что ему нужна операция на сердце, Эндрю Росс, M.Д. знал, что для того, чтобы заботиться о своих пациентах, он должен заботиться о себе. Для этого он обратился в клинику Мэйо. В прошлом году Эндрю Росс, доктор медицины, 44-летний гастроэнтеролог, привыкший к своей роли врача, […]
24 октября 2020 г.
Турбулентная причина двусторонней пневмонии
ИСТОРИЯ КОРПУСА
Женщина 62 лет обратилась с жалобами на прогрессирующую боль в груди, усиливающуюся при вдохе, продуктивный кашель и лихорадку в течение 2 дней.Более того, за последние 3 месяца она похудела на 12 кг, и у нее была ночная потливость. В этот период у нее был фолликулит подмышечной впадины. В ее медицинском анамнезе указан сахарный диабет II типа, гипертония и анемия. Трансторакальная эхокардиография, проведенная 4 года назад, выявила нарушения кровотока в легочной артерии и перегрузку объемом левого желудочка. Лекарства пациентов включали метформин, инсулин, гидрохлоротиазид, симвастатин, метопролол, феррофумерат и витамин B.
При медицинском осмотре был замечен бледный и кахексический пациент. Температура ее тела была 39 ° C, частота пульса 104 уд / мин -1 , частота дыхания 20 вдохов / мин -1 и артериальное давление 160/65 мм рт. При аускультации грудной клетки были выявлены нормальные звуки дыхания, систолический шум 2/6 в правой парастернальной области и непрерывный шум 1/6 в левой парастернальной области. В остальном медицинский осмотр был нормальным.
Обзор исследований представлен в таблице 1⇓.Рентгенограмма грудной клетки была сделана при поступлении (рис. 1⇓), а компьютерная томография (КТ) с контрастным усилением — до и после лечения (рис. 2⇓ и 3⇓, соответственно). Компьютерная томография была также сделана в паренхиматозных условиях (рис. 4⇓).
Рис. 1–Рентгенограмма грудной клетки при поступлении: большая правая воротная часть и уплотнения в обеих нижних долях.
Рис. 2—Изображения компьютерной томографии с контрастным усилением при поступлении. Показана сагиттальная плоскость, реконструированная по данным поперечных срезов.Стрелка А указывает на открытый артериальный проток, соединяющий дугу аорты с легочной артерией. Стрелка B указывает на помутнения легочного ствола, указывающие на наличие растительности. На дуге аорты видна кальцинированная область.
Рис. 3—Изображения компьютерной томографии с контрастным усилением через 4 месяца после лечения антибиотиками. Показана сагиттальная плоскость, реконструированная по данным поперечных срезов. Стрелка указывает на открытый артериальный проток, соединяющий дугу аорты с легочной артерией.Растения в легочном стволе исчезли.
Рис. 4—Компьютерная томография основания легкого. В нижних долях есть двусторонние уплотнения.
Таблица 1–Сводка исследований
ПЕРЕД ПЕРЕКЛЮЧЕНИЕМ СТРАНИЦЫ, ИНТЕРПРЕТАЦИЯ ИСТОРИИ ПАЦИЕНТА, РАДИОГРАФИИ ГРУДИ, КТ-СКАНИРОВАНИЯ С УСИЛЕННЫМ КОНТРАСТОМ И КТ-СКАНИРОВАНИЯ, И ПРЕДЛОЖИТЕ ДИАГНОСТИКУ.
ИНТЕРПРЕТАЦИЯ
Пациент в анамнезе имел усталость, лихорадку, потерю веса и анемию, которые могли быть вызваны хронической инфекцией или злокачественным новообразованием.Рентгенограмма грудной клетки при поступлении показала большие правые ворота и уплотнения в обеих нижних долях (рис. 1⇑). КТ подтвердила открытый артериальный проток (ОАП), который подозревался при трансторакальной эхокардиографии 4 года назад, а также увеличение правой и левой легочных артерий. Кроме того, были обнаружены помутнения легочного ствола, указывающие на наличие растительности. В дуге аорты обнаружен кальцинированный участок, который может указывать на перенесенную инфекцию (рис. 2⇑). Признаков эмболии легочных артерий не наблюдалось.В паренхиме присутствовали двусторонние уплотнения в нижних долях (рис. 4⇑). Трансэзофагеальная цветная допплерэхокардиография показала гипердинамический левый желудочек, увеличенное левое предсердие, турбулентный кровоток в легочной артерии и аномальный кровоток из аорты в легочную артерию через КПК.
Диагноз: Легочный эндартериит на фоне ОАП и последующей метастатической легочной инфекции.
У пациента вегетация была выявлена на компьютерной томографии в легочном стволе ниже ОАП.В этой области эндотелий повреждается турбулентной струей. Поврежденный эндотелий очень восприимчив к инфекциям с ростом растений, особенно в случае рецидивирующей бактериемии от источника инфекции. Эти растения могли образовать септические эмболы, вызывающие внезапное ухудшение симптомов и легочные уплотнения. Таким образом, визуализирующие исследования в сочетании с клинической картиной позволили диагностировать легочный эндартериит при наличии КПК и последующей метастатической легочной инфекции.
ЛЕЧЕБНО-КЛИНИЧЕСКИЙ КУРС
Первоначально пациент получал амоксициллин-клавуланат 750 мг три раза в день. в течение первых 6 дней. Его заменили на пенициллин G 12 × 10 6 МЕ · день -1 в / в. непрерывно и гентамицин 260 мг раз в день. в.в. в течение 4 недель, когда диагноз легочного эндартериита считался наиболее вероятным. Многочисленные посевы крови были отрицательными. Кроме того, ее лечили низкомолекулярным гепарином и кумарином.В результате этого лечения нормализовались температура и С-реактивный белок. Однако через 2 недели лечения у пациента снова появился кашель и жар. В образце бронхоальвеолярного лаважа была обнаружена β-лактамаза, продуцирующая Moraxella catarrhalis , устойчивую к пенициллину. Поэтому лечение антибиотиками было продлено с помощью цефуроксима в / в. на 1 неделю. Рентгенограмма грудной клетки показала новое помутнение в левом верхнем поле, а позитронно-эмиссионная томография-КТ показала повышенную активность в этой области.Помутнение в легочной артерии исчезло. Через 4 недели пациент был выписан без каких-либо симптомов со стороны грудной клетки или лихорадки. Во время наблюдения пациент жаловался на утомляемость, без рецидива инфекции, а компьютерная томография показала, что ОАП не помутнен (рис. 3⇑). Пациенту было выполнено чрескожное закрытие артериального протока с использованием устройства для закрытия протока Amplatzer (AGA Medical Corporation, Golden Valley, MN, США) через 8 месяцев. Успешное закрытие ОАП было подтверждено цветной допплеровской эхокардиографией, которая не показала остаточного шунта из дуги аорты в легочный ствол.После закрытия больная жалоб не предъявляла.
ОБСУЖДЕНИЕ
В представленном случае у 62-летнего пациента выявлены эндоваскулярные осложнения ОАП. Артериальный проток — это шунт, соединяющий дугу аорты с легочной артерией. Он является частью сосудистой системы плода, позволяя крови проходить через заполненные жидкостью легкие. Обычно проток закрывается, когда новорожденный ребенок начинает дышать, и полностью закрывается в течение первых 10 дней после рождения.Однако нередки случаи, когда проток полностью не закрывается. Это сосудистое состояние, PDA, является фактором риска легочного эндартериита, эмболии, легочной гипертензии и сердечной недостаточности.
В представленном случае ОАП был диагностирован на 4 года раньше с соотношением легочного и системного кровотока <1,5. Однако пациент в возрасте 60 лет отказался от дальнейшего обследования для оценки и закрытия протока из-за отсутствия симптомов.
В первой половине 21 века легочный эндартериит был частой причиной смерти пациентов с КПК 1.Благодаря введению антибиотиков и развитию хирургических методов закрытия ОАП, риск эндартериита и смертности существенно снизился и в настоящее время встречается очень редко. 2. В недавнем исследовании в Швеции были проанализированы записи 281 пациента с ОАП. в общей сложности 1196 лет подвержены риску инфекционного эндартериита. В ходе исследования не было обнаружено ни одного случая эндартериита 3. В связи с этим возник вопрос, показано ли закрытие КПК с единственной целью профилактики инфекционного эндартериита 3, 4.
Сообщалось о нескольких случаях ОАП, сопровождающегося легочным эндартериитом, с последующей легочной инфильтрацией или без нее 5–11. Посев крови в этих отчетах о случаях выращивал видов Gamella , Streptococcus группы D, Streptococcus mitis , S. capitis, S. millei и S. viridans . В нашем случае ни один вид не рос в многочисленных посевах крови, вероятно, потому, что пациентка лечилась пероральными антибиотиками ее терапевтом. Пациент лечился антибиотиками в течение 4 недель, как рекомендовано при эндокардите lenta с отрицательными посевами, с i.v. пенициллин и гентамицин 12. В образце, полученном с помощью брохоальвеолярного лаважа, было выделено Moraxella catharralis . Этот патоген, вероятно, не был причиной эндартериита ОАП, поскольку он редко разрастается инвазивно.
Эндокардит в целом почти всегда вызывается рецидивирующей бактериемией от источника инфекции и спонтанно у <1% 13. В нашем случае мы можем только предполагать источник инфекции. Начало хронических жалоб пациентки сопровождалось фолликулитом в подмышечной впадине, к которому она могла быть более восприимчива из-за диабета.Неизвестно, является ли диабет дополнительным фактором риска инфекционного эндартериита. Однако случай с комбинацией диабета, КПК и инфекционного легочного эндартериита с последующими легочными инфильтратами был описан ранее 5.
Дифференциальный диагноз включал не только инфекционный эндартериит и последующую эмболию, но и эмболии, вызванные неинфекционным воспалительным процессом в области протока ОАП, злокачественной опухолью или аутоиммунным заболеванием.
Диагностика инфекционного эндартериита затруднена при отрицательном посеве крови.Не все возбудители эндокардита растут в крови, например, Bartonella spp, Coxiella spp, Chlamydia spp и виды группы HACEK привередливы 14, 15. В случае отрицательных посевов крови маркеры воспаления могут различать инфекционные и неинфекционные причины заболеваний. Для установления диагноза инфекционный эндартериит могут быть полезны С-реактивный белок, прокальцитонин, интерлейкин-6, фактор некроза опухоли-α и интерлейкин-1β в сыворотке крови, поскольку эти маркеры значительно увеличены по сравнению со здоровыми контрольными субъектами.Из этих маркеров С-реактивный белок имеет наилучшую прогностическую ценность 16. Повышение С-реактивного белка в сочетании с лихорадкой, по-видимому, указывает на инфекционную причину. Имея эту информацию, мы считаем менее вероятными неинфекционные эмболии.
Быстрое исчезновение помутнения после начала лечения выступает против злокачественной опухоли. У пациентки были положительные титры антиядрышковых антител, что могло указывать на аутоиммунную причину ее жалоб.Однако пациент не получал никакого иммуномодулирующего лечения и ответил на антибиотики полной нормализацией С-реактивного белка и температуры тела.
Клиническое течение, анализ крови и реакция на терапию, а также результаты визуализирующих исследований почти подтвердили диагноз: инфекционный эндартериит и последующие тромбоэмболии легочной артерии, хотя мы не культивировали патогенный микроорганизм. Однако положительный посев крови не является обязательным для диагностики легочного эндартериита, поскольку он основан на определении, используемом в ретроспективном исследовании, в котором ОАП, сопровождающийся легочным эндартериитом, определяется как клиническая картина, обычно связанная с эхокардиографической вегетацией, или положительный посев крови 3 .
В заключение, легочный эндартериит — редкое опасное для жизни осложнение открытого артериального протока. В случае необъяснимой лихорадки у пациента с ранее существовавшим открытым артериальным протоком следует рассмотреть и исследовать легочный эндартериит с помощью эхокардиографии, компьютерной томографии, ангиограммы или магнитно-резонансной томографии и посева крови. Как следствие септической эмболии могут развиться легочные инфильтраты.
Заявление о заинтересованности
Не объявлено.
Список литературы
- ↵
Кэмпбелл М. Естественная история постоянного артериального протока. Br Heart J 1968; 30: 4–13.
- ↵
Awadallah SM, Kavey RE, Byrum CJ, et al. Изменение характера инфекционного эндокардита в детстве. Am J Cardiol 1991; 68: 90–94.
- ↵
Тилен У., Астром-Олссон К. Оправдывает ли риск инфекционного эндартериита рутинное закрытие открытого артериального протока ?.Eur Heart J 1997; 18: 503–506.
- ↵
Салливан ID. Запатентованный артериальный проток: когда его закрывать ?. Arch Dis Child 1998; 78: 285–287.
- ↵
Онджи К., Мацуура В. Легочный эндартериит и последующая тромбоэмболия легочной артерии, связанная с клинически бессимптомным открытым артериальным протоком. Intern Med 2007; 46: 1663–1667.
Rivera IR, Moises VA, Brandao AC, et al. Открытый артериальный проток и эндартериит легочной артерии. Арк Брас Кардиол 1997; 69: 335–338.
Bilge M, Uner A, Ozeren A, et al. Легочный эндартериит и последующая эмболизация легкого как осложнение открытого артериального протока — отчет о клиническом случае. Ангиология 2004; 55: 99–102.
Vargas-Barron J, Attie F, Buendia-Hernandez A, et al. Эхокардиографическое распознавание эндартериита легочной артерии открытого артериального протока.Am Heart J 1985; 109: 368–370.
Lankipalli RS, Lax K, Keane MG, et al. Изображения в сердечно-сосудистой медицине. Инфицированный открытый артериальный проток. Обращение 2005 г .; 112: e364 – e365.
Celebi A, Erdem A. Cokugras Het al. Инфекционный эндартериит у 2-месячного младенца, связанный с безымянным открытым артериальным протоком. Анадолу Кардиол Дерг 2007; 7: 325–327.
- ↵
Янык А., Еткин Е., Ллери М., и др. Вегетация, вызванная Streptococcus viridans в легочной артерии у ребенка с открытым артериальным протоком. Инт Дж. Кардиол, 2000; 72: 189–191.
- ↵
Эллиотт Т.С., Фоверакер Дж., Гулд Ф.К., и др. Рекомендации по лечению эндокардита антибиотиками у взрослых: доклад Рабочей группы Британского общества антимикробной химиотерапии. Журнал Antimicrob Chemother 2004; 54: 971–981.
- ↵
Durack DT.Профилактика инфекционного эндокардита. N Engl J Med 1995; 332: 38–44.
- ↵
Houpikian P, Raoult D. Эндокардит с отрицательным посевом крови в справочном центре: этиологический диагноз 348 случаев. Медицина (Балтимор) 2005; 84: 162–173.
- ↵
Das M, Badley AD, Cockerill FR, et al. Инфекционный эндокардит, вызванный микроорганизмами HACEK. Анну Рев Мед 1997; 48: 25–33.
- ↵
Watkin RW, Harper LV, Vernallis AB, et al. Провоспалительные цитокины IL6, TNF-α, IL1β, прокальцитонин, липополисахаридсвязывающий белок и C-реактивный белок при инфекционном эндокардите. J Infect 2007; 55: 220–225.
Заболевание сонной артерии — Harvard Health
Мозгу требуется постоянный приток кислорода. Большая часть его поступает из богатой кислородом крови, поступающей по сонным артериям. Они проходят от основной артерии тела, аорты, вверх по обе стороны шеи (где их пульс ощущается с любой стороны трахеи или трахеи) в мозг.
Бляшка, содержащая холестерин, может сузить сонную артерию. Это называется заболеванием сонной артерии.
Большой налет может замедлить приток крови к мозгу. Еще большее беспокойство вызывает разрыв зубного налета. Сгусток крови, образующийся для закрытия разрыва, может попасть в мозг, вызывая временную ишемическую атаку (мини-инсульт) или инсульт.
Симптомы болезни сонной артерии
Заболевание сонной артерии часто не имеет признаков или симптомов до тех пор, пока не сильно сужается или не блокируется сонная артерия.Признаки и симптомы могут включать шум (бро-ЭЭ), преходящую ишемическую атаку или инсульт.
Сужение сонной артерии вызывает турбулентный кровоток. Подобно воде, текущей по бурлящему ручью, турбулентный поток в кровеносном сосуде вызывает шум. Ваш врач может услышать этот шум, называемый шумом, путем прослушивания ваших сонных артерий через стетоскоп. К сожалению, многие артерии с ушибами имеют вполне адекватный кровоток, в то время как некоторые сильно суженные артерии несут кровь беззвучно.
Преходящая ишемическая атака, также известная как мини-инсульт, может быть первым признаком болезни сонной артерии. Мини-инсульт очень похож на полноценный инсульт, за исключением того, что симптомы проходят сами по себе в течение 24 часов.
Симптомы транзиторной ишемической атаки включают:
- внезапная слабость или онемение лица, рук или ног, часто с одной стороны тела
- Проблемы с движением руки или ноги
- Проблемы с речью или пониманием речи
- внезапное ухудшение зрения одним или обоими глазами
- внезапное головокружение или потеря равновесия
Мини-удар — это предупреждающий знак о том, что возможен удар.Приблизительно у 1 из 3 человек, у которых впоследствии возникли мини-инсульты, инсульт.
У некоторых людей инсульт является первым симптомом заболевания сонной артерии. Симптомы инсульта такие же, как и у мини-инсульта, но он может привести к долгосрочным повреждениям, таким как паралич, проблемы со зрением или речью и даже смерть.
Диагностика болезни сонной артерии
Отправной точкой для выявления болезни сонной артерии является ультразвуковое исследование. Он использует звуковые волны для создания изображений сонных артерий.Ультразвук сонных артерий — хороший способ определить серьезное сужение сонной артерии, но он менее точен для более легких закупорок.
Магнитно-резонансная ангиография и компьютерная томографическая ангиография позволяют получать подробные изображения закупорки сонной артерии. Эти сканирования создают высококачественные изображения сонных артерий. Компьютерная томографическая ангиография включает облучение; магнитно-резонансной ангиографии нет.
Каротидная ангиография — это инвазивный тест, который требует введения тонкой трубки, называемой катетером, в кровеносный сосуд на руке или ноге и осторожного проведения ею до сонных артерий.После установки катетер вводит краситель в артерии. Движение красителя по сонным артериям фиксируется серией рентгеновских лучей.
Лечение болезни сонной артерии
Заболевание сонной артерии можно лечить медикаментами или процедурой по удалению сужения. В обоих случаях цель — предотвратить инсульт.
Медикаментозная терапия предполагает прием лекарств для защиты артерий. К ним относятся:
- аспирин или другое антитромбоцитарное средство для предотвращения образования тромбов
- статин, снижающий уровень холестерина, для лечения атеросклероза с закупоркой артерий и стабилизации бляшек, заполненных холестерином
- при необходимости одно или несколько препаратов для снижения артериального давления
Доступны два варианта открытия артерии:
- каротидная эндартерэктомия.Во время этой операции хирург открывает закупоренную сонную артерию и удаляет бляшки, заполненные холестерином.
- ангиопластика со стентированием. В этой процедуре врач вставляет тонкую проволоку, называемую катетером, в кровеносный сосуд на ноге или шее и осторожно вводит ее в суженную сонную артерию. Когда катетер находится на месте, крошечный баллон на его конце расширяется, сглаживая бляшку. Баллон расширяет сетку из проволочной сетки, называемую стентом, и проталкивает ее в стенки артерии. Это удерживает артерию открытой после удаления баллона и катетера.
Медикаментозная терапия воздействует на атеросклероз, являющийся основной причиной заболевания сонной артерии, по всем сонным артериям и остальным частям тела. Процедура лечит только одно сужение. Кроме того, каротидная эндартерэктомия и ангиопластика могут вызвать инсульт или вызвать другие побочные эффекты, хотя риск невелик, если это делает опытный врач в больнице, которая часто выполняет эту процедуру.
Два ключевых фактора могут помочь сделать правильный выбор: наличие или отсутствие симптомов и степень сужения сонной артерии.
Лица без симптомов
Людям с заболеванием сонной артерии, не вызывающим никаких симптомов, лучше всего, по крайней мере, на начальном этапе, медикаментозное лечение, особенно если сужение менее 70%.
Лица, у которых заболевание сонной артерии не вызывает никаких симптомов, но сужение которого превышает 70%, могут выбрать лечение или процедуру открытия артерии.
Лица с симптомами
Лица с заболеванием сонной артерии, перенесшие преходящую ишемическую атаку или инсульт, должны рассматриваться для процедуры по открытию или очистке закупоренной сонной артерии, если сужение превышает 50%.Пациенты с тяжелым сужением (от 70% до 99%) получают наибольшую пользу, но пациенты с умеренным сужением (от 50% до 69%) также могут получить некоторую защиту от будущих инсультов.
Поделиться страницей:
Заявление об отказе от ответственности:
В качестве услуги для наших читателей Harvard Health Publishing предоставляет доступ к нашей библиотеке заархивированного содержимого. Обратите внимание на дату последнего обзора или обновления всех статей. Никакой контент на этом сайте, независимо от даты, никогда не должен использоваться вместо прямого медицинского совета вашего врача или другого квалифицированного клинициста.
Шумы в сердце | Сидарс-Синай
Не то, что вы ищете?Что такое шум в сердце?
Сердце издает звуки во время биения. Эти звуки появляются как сердечные клапаны открываются и закрываются, позволяя крови течь через сердце. Шум в сердце это дополнительный шум, слышимый во время сердцебиения. Шум возникает, когда кровь не плавно течь через сердце.
Шумы в сердце могут быть невинными (безвредными) или ненормальными (вызванными проблемы с сердцем). Типы шумов:
- Систолический шум. Это случается во время сокращения сердечной мышцы. Систолические шумы делятся на выбросы шумы (из-за кровотока через суженный сосуд или неправильный клапан) и регургитирующие шумы (обратный ток крови в одну из камер сердца).
- Диастолический шум. Это случается когда сердечная мышца расслабляется между ударами. Диастолические шумы от сужение (стеноз) митрального или трехстворчатого клапанов или регургитация аортальные или легочные клапаны.
- Непрерывный шум. Это случается на протяжении сердечного цикла.
Что вызывает шум в сердце?
Невинный (также называемый функциональным) шум в сердце может быть нормальным находка для многих людей. Это также может быть вызвано:
- Лихорадка
- Упражнение
- Беременность
- Низкое количество эритроцитов (анемия)
- Гиперактивная щитовидная железа
- В период быстрого роста детей
Обычно кровь течет из одной камеры сердца в другую и клапаны плотно закрываются, чтобы кровь не оттекала назад.Аномальное сердце шум может быть вызван проблемами с сердцем, такими как:
- Поврежденный или больной клапан. клапан может быть слишком узким, чтобы кровь могла легко проходить через него. Или это может быть проблемы с открытием или закрытием, а также может течь кровь назад.
- Отверстие в сердце (перегородка дефект). Это проблема со структурой сердца, которую человек родился с (врожденным).Это вызывает утечку крови через стену, что обычно разделяет левую и правую части сердца.
- Утолщение стенок насосные камеры сердца (гипертрофическая обструктивная кардиомиопатия)
Эти условия могут вызвать турбулентное движение крови через сердце. Этот поток издает необычные звуки или шепот, который слышен с помощью стетоскопа. когда ваш лечащий врач проводит медицинский осмотр.
Каковы симптомы шума в сердце?
Шумы в сердце не часто вызывают симптомы. Их обычно можно найти когда ваш лечащий врач прислушивается к вашему сердцу по другой причине. Люди с аномальным шумом в сердце могут иметь симптомы проблемы, вызывающей шум. Они могут включать:
- Чувство слабости или усталости
- Одышка, особенно при физической нагрузке
- Боль в груди
- Быстрое, учащенное или пропадающее сердцебиение
- Отек лодыжек, стоп или живота (живота)
- Чувство головокружения или обморока
Как диагностируется шум в сердце?
Чтобы диагностировать шум в сердце, ваш лечащий врач сначала спросите об истории вашего здоровья.Они также будут слушать ваше сердце. Ваше здоровье Провайдер может услышать шум с помощью стетоскопа.
Некоторые шумы лучше всего слышны при прослушивании на передней панели грудь. Другие лучше всего слышны при прослушивании со стетоскопом на спине. Ваш врач может попросить вас задержать дыхание, чтобы звук вашего сердца биение можно услышать без звуков вашего дыхания. Вас также могут попросить лягте на бок или встаньте и присядьте.Это чтобы увидеть, как покои сердца и клапаны реагируют на усиление кровотока через камеры сердца и сердце клапаны.
Шумы в сердце чаще всего бывают совершенно нормальными. Но иногда они может быть признаком проблемы с сердцем. Так что вам также могут понадобиться некоторые тесты. Это может помочь диагностировать проблему с сердечным клапаном и исключить любое другое заболевание, которое у вас может быть:
- Рентген грудной клетки. Этот визуальный тест смотрит на ваше сердце и легкие.
- Электрокардиограмма. Этот тест показывает ритм сердцебиения.
- Катетеризация сердца. Это тест заглядывает в сердце. Помогает измерять давление в камерах, проверяет герметичность клапанов и ищет проблемы в сердечных артериях.
- Трансторакальная эхокардиограмма (эхо). Это простой и безболезненный тест, позволяющий отразить безвредный звук. волны от сердца. Эти звуковые волны становятся изображениями на видеоэкране. Ваш После этого врач сможет увидеть движущееся изображение вашего сердца. Этот тест показывает как работают клапаны. Он может подтвердить, сужен ли клапан или течет.Это может также показать размер камер и нормально ли качает сердечная мышца.
- Чреспищеводное эхо (TEE). Это это особый тип эха. Он может предоставить еще более подробную информацию о ваши сердечные клапаны. Но TEE несколько более сложен, чем поверхностное эхо, поскольку он требуется, чтобы в пищевод был введен зонд. Таким образом, поверхностное эхо часто бывает первый тест сделан.
Как лечить шум в сердце?
Невинный шум в сердце не требует лечения, если он отсутствует. явная причина, например анемия. В таких случаях лечение основной причины должен вылечить ропот. В некоторых случаях невинный шум в сердце может уйти на его собственный.
Лечение аномального шума в сердце зависит от его причины.Возможные варианты:
- Лекарства, облегчающие симптомы
- Процедуры или хирургические вмешательства по исправлению или замене больного или поврежденный сердечный клапан
- Операции или операции по исправлению сердечной недостаточности
Какие возможные осложнения при шуме в сердце?
Невинный шум в сердце не имеет осложнений.Осложнения аномальный шум в сердце зависит от причины. Возможные осложнения включать:
- Сердечная недостаточность, когда сердце настолько слабо, что перестает качать кровь кровь хорошо
- Инфекция сердечных клапанов или внутренней оболочки (инфекционная эндокардит)
- Тромбы и инсульт
- Обморок
- Сердечный приступ
- Внезапная остановка сердца, когда сердце внезапно останавливается избиение
Когда мне следует позвонить своему врачу?
Немедленно позвоните своему врачу, если у вас есть эти:
- Боль в груди, очень похожая на ту, что вы чувствовали мимо
- Легкая одышка
- Легкое ощущение учащенного сердцебиения (учащенное сердцебиение)
- Лихорадка 100.4 ° F (38 ° C) или выше, или по указанию вашего поставщик медицинских услуг
- Симптомы, которые не проходят при лечении или исчезают худший
- Новые симптомы
Позвоните 911
Позвонить 911 или немедленно обратитесь за медицинской помощью, если происходит любое из них:
- Новая, сильная или другая боль в груди
- Сильная одышка
- Сильное сердцебиение
- Чувство головокружения или потеря сознания
Основные сведения о шумах в сердце
- Шум в сердце — это дополнительный шум, слышимый во время сердцебиения.Шум возникает, когда кровь не течет плавно через сердце.
- Шумы в сердце могут быть невинными (безвредными) или аномальными (вызванными из-за проблемы с сердцем).
- Некоторые причины: лихорадка, анемия или заболевание сердечного клапана.
- Шумы в сердце не часто вызывают симптомы.
- Медицинский работник может услышать шум с помощью стетоскоп.
- Невинный шум в сердце не требует лечения. An ненормальный можно лечить с помощью лекарств или хирургического вмешательства.
Следующие шаги
Советы, которые помогут вам получить максимальную пользу от посещения вашего врача провайдер:
- Знайте причину вашего визита и то, что вы хотите случаться.
- Перед визитом запишите желаемые вопросы ответил.
- Возьмите с собой кого-нибудь, кто поможет вам задать вопросы и помните, что вам говорит ваш провайдер.
- При посещении запишите название нового диагноза и любые новые лекарства, методы лечения или тесты. Также запишите все новые инструкции ваш провайдер дает вам.
- Узнайте, почему прописано новое лекарство или лечение и как это поможет вам. Также знайте, какие бывают побочные эффекты.
- Спросите, можно ли вылечить ваше состояние другими способами.
- Знайте, почему рекомендуется тест или процедура и какие результаты могут означать.
- Знайте, чего ожидать, если вы не примете лекарство или тест или процедура.
- Если у вас назначена повторная встреча, запишите дату, время и цель этого визита.
- Узнайте, как вы можете связаться с вашим провайдером, если у вас вопросов.
Пролапс митрального клапана | Сидарс-Синай
Не то, что вы ищете?Что такое пролапс митрального клапана?
Митральный клапан позволяет крови поток из левого предсердия в левый желудочек сердца.Пролапс митрального клапана (ПМК) — выпуклость (пролапс) одного или обоих лоскутов (створок) митрального клапана в левое предсердие при сокращении сердца. Когда створки не закрываются должным образом, кровь течет назад. Это называется срыгиванием. Срыгивание может вызвать шум в сердце, ненормальный звук в сердце, вызванный турбулентным кровотоком. Когда срыгивание в настоящее время, как правило, легкая. Но со временем может стать хуже.
Митральный клапан расположен между левое предсердие и левый желудочек и имеет 2 лоскута.Обычно створки плотно прилегают закрывается небольшими сухожилиями или «шнурами», которые соединяют лоскуты с мышцами сердца. Это закрытие предотвращает обратный ток крови. В MVP закрылки увеличиваются и тянутся внутрь к левому предсердию, иногда «ломаясь» при сокращении сердца. Это может привести к обратному току или срыгиванию крови в левое предсердие.
MVP обычно не требуется лечить, потому что это редко бывает серьезным заболеванием и не повреждает сердце.Тем не менее, рекомендуется регулярно посещать врача.
Что вызывает MVP?
Причина MVP неизвестна, но считается, что большинство случаев передаются по наследству. Есть 2 формы MVP: первичная и вторичный.
Первичный MVP
Первичный MVP означает митральный клапан неисправен из-за одного или нескольких из следующих изменений:
- Одна или обе заслонки слишком большой и толстый
- Поверхность клапана в рубцах
- Связки сухожилий тоньше или длиннее, чем должно быть
- Отложения фибрина на закрылки
Первичный MVP чаще всего изолированное заболевание.Но это может быть связано с другими проблемами клапана или скелета. Некоторые редкие экземпляры MVP являются наследственными.
Вторичный MVP
Во вторичном MVP, другой заболевание связано с ПМК. Часто створки клапана не утолщены. Происходит пролапс по другим причинам. Выпадение может быть от:
- Урон от уменьшения количества крови поток от ишемической болезни сердца к мышцам, прикрепленным к связкам сухожилий
- Функциональные изменения в сердце мышца
- Повреждение клапанных конструкций сердечным приступом, ревматической болезнью сердца, инфекцией клапана или гипертрофией кардиомиопатия.Гипертрофическая кардиомиопатия — это когда левый желудочек сердце больше обычного.
- Повреждение, вызванное заболеванием соединительной ткани, таким как Марфан синдром
Кто подвержен риску MVP?
MVP влияет как на людей, так и на пол. всех возрастов. Факторы, которые могут увеличить риск MVP, включают:
- Болезнь Грейвса (состояние, при котором поражает щитовидную железу)
- Определенные заболевания соединительной ткани, такие как синдром Марфана
- Сколиозы и другие скелеты проблемы
- Некоторые виды мышечной дистрофии
Каковы симптомы MVP?
MVP может не вызывать никаких симптомов.Симптомы могут различаться в зависимости от степени выпадения. Наличие симптомов не обязательно соответствует серьезности MVP.
Это наиболее частые симптомы. MVP:
- Быстрое или нерегулярное сердцебиение (сердцебиение). Это может быть результатом нерегулярного сердцебиения или просто ощущение закрытия клапана при нормальном сердечном ритме.
- Боль в груди. Боль в груди связана с ПМК отличается от боли в груди, связанной с ишемической болезнью сердца. Обычно боль в груди не похожа на классическую стенокардию, например, боль при физической нагрузке, но может случиться часто могут быть очень неудобными и могут повлиять на качество вашей жизни.
- Беспокойство
- Гипервентиляция
- Непереносимость физических упражнений
- Головокружение
В зависимости от степени тяжести митральная регургитация или утечка, левое предсердие или левый желудочек могут увеличиться, приводящие к симптомам сердечной недостаточности.Эти симптомы включают слабость, усталость, головокружение и одышка.
Симптомы митрального клапана пролапс может выглядеть как другие заболевания или проблемы. Всегда обращайтесь в медицинское учреждение провайдер для диагностики.
Как диагностируется пролапс митрального клапана?
У вас может не быть заметного симптомы. Ваш врач может услышать щелчок или шепот во время обычного медицинского осмотра.В «щелчок» создается за счет защелкивания вытянутых створок друг о друга во время сокращение. Шум вызван утечкой крови обратно в левое предсердие. Этот может быть единственным признаком MVP.
Вместе с полным медицинским анамнез и физический осмотр, ваш поставщик может назначить эти тесты для диагностики MVP:
- Электрокардиограмма (ЭКГ). Этот тест фиксирует силу и время электрической активности сердца.Он показывает ненормальные ритмы и может иногда обнаруживают поражение сердечной мышцы. Маленькие датчики прикреплены к вашей коже, чтобы улавливать электрическая активность.
- Рентген грудной клетки. Рентген можно сделать, чтобы проверьте свои легкие и посмотрите, не увеличилось ли ваше сердце.
- Трансторакальная эхокардиограмма (эхо или TTE). Это неинвазивный тест, в котором используются звуковые волны для оценки сердечного ритма. камеры и клапаны.Звуковые волны эха создают изображение на мониторе в виде ультразвуковой датчик проводится над грудной клеткой над сердцем. Эхокардиография — это самый полезный диагностический тест для MVP.
При более тяжелых симптомах другое тесты могут быть сделаны. Сюда могут входить:
- Стресс-тест. Это также называется беговая дорожка или ЭКГ с нагрузкой. ЭКГ выполняется, когда вы ходите по беговой дорожке, чтобы контролировать сердце во время тренировки.Также проверяются показатели дыхания и артериального давления.
- Катетеризация сердца. С этим процедура, рентген делается после введения контрастного вещества (красителя) в артерию искать любые сужения, закупорки или другие изменения в определенных артериях. В также можно проверить работу сердца и клапанов.
- МРТ сердца. Это визуальный тест который делает подробные снимки сердца.Его можно использовать для более точного просмотра на сердечных клапанах и сердечной мышце или для подготовки к операции на сердечном клапане.
Как лечится пролапс митрального клапана?
MVP обычно не требуется лечить, потому что это редко бывает серьезным заболеванием и не повреждает сердце. Рекомендуются регулярные осмотры у врача.
Если у вас изменения сердечного ритма, вам могут потребоваться лекарства, контролирующие учащенное сердцебиение или нерегулярное сердцебиение. В большинстве случаях вам также необходимо ограничить употребление стимуляторов, таких как кофеин и сигареты, чтобы контролировать симптомы.
Если у вас фибрилляция предсердий или тяжелое увеличение левого предсердия, может потребоваться лечение антикоагулянтом (кровь тоньше), чтобы предотвратить образование сгустков. Это может быть в форме аспирина, варфарина. терапия или другие новые препараты для разжижения крови
Если у вас есть симптомы головокружения или обморока, важно пить много жидкости, чтобы не обезвоживаться.
Если тяжелая митральная регургитация из-за гибкой митральной створки, разрыва (разрыва) связок или чрезмерного удлинения клапана, вам может потребоваться транскатетерное восстановление митрального клапана, хирургическое вмешательство или клапан замена.
Какие возможные осложнения митрального клапана пролапс?
Редко бактерии, попадающие в кровоток может вызвать эндокардит, инфекцию внутренней оболочки сердца камеры и клапаны.Этот риск выше у людей с ПМК, потому что деформированный митральный лоскут клапана может привлечь бактерии, попавшие в кровоток. Инфекции десен и зубов кариес может вызвать эндокардит, поэтому регулярная чистка зубов зубной нитью может помочь предотвратить это. У вас может быть высокий риск эндокардита, если вам заменили клапан. Возможно, вам придется принимать антибиотики перед стоматологической работой и некоторыми видами хирургических вмешательств.
Когда мне следует позвонить своему врачу?
Позвоните своему врачу, если ваши симптомы ухудшаются или появляются новые симптомы.
Основные сведения о пролапсе митрального клапана
- Пролапс митрального клапана (ПМК) — это выпячивание (пролапс) одного или обоих лоскутов митрального клапана в левое предсердие во время сокращения сердца. Одна или обе створки не закрываются должным образом, позволяя крови течь назад (срыгивание).
- Некоторые вещи, которые могут увеличить риск MVP включают болезнь Грейвса, некоторые заболевания соединительной ткани, такие как болезнь Марфана. синдром, сколиоз и другие проблемы со скелетом, а также некоторые типы мышечных дистрофия.
- Люди с MVP часто щелкают или шепот, который слышен во время обычного медицинского осмотра.
- MVP обычно не требуется лечится, потому что это редко бывает серьезным заболеванием и не повреждает сердце.
- Люди с нарушениями сердечного ритма могут необходимо лечиться лекарствами для контроля тахикардии (учащенного сердечного ритма).
- MVP обычно безвреден и не сократить продолжительность жизни.
Следующие шаги
Советы, которые помогут получить максимальную отдачу от визит к вашему лечащему врачу:
- Знайте причину вашего визита и что вы хотите.
- Перед визитом запишите вопросы, на которые вы хотите получить ответы.
- Возьмите с собой кого-нибудь, чтобы помочь вам спросить вопросы и запомните, что вам говорит ваш провайдер.
- При посещении запишите имя новый диагноз и любые новые лекарства, методы лечения или тесты. Также запишите любые новые инструкции, которые дает вам ваш провайдер.
- Знайте, почему новое лекарство или лечение прописан, и как он вам поможет. Также знайте, какие бывают побочные эффекты.
- Спросите, можно ли вылечить ваше состояние другими способами.
- Знайте, почему тест или процедура рекомендуются и что могут означать результаты.
- Знайте, чего ожидать, если вы не примете лекарство или пройти тест или процедуру.
- Если вам назначен повторный прием, запишите дату, время и цель визита.
- Узнайте, как можно связаться со своим провайдером Если у вас есть вопросы.
(PDF) Шумовое поле в грудной клетке человека из-за турбулентного потока в более крупном кровеносном сосуде
ШУМОВОЕ ПОЛЕ В ГРУДЕ ЧЕЛОВЕКА 283
Благодарности
Автор с благодарностью отмечает финансовую поддержку Фонда Александра фон
Гумбольдта (Германия ) и полезные комментарии профессора П.
Költzsch при обсуждении этой работы.
Ссылки
1. Гидденс, Д.П., Мабон, Р.Ф. и Кассанова, Р.А., Измерение неупорядоченного кровотока дистальнее
субтотального стеноза сосудов в грудной аорте собак. Circ. Res. 39 (1976) 112–119.
2. Тобин, Р.Дж. и Чанг, И.Д., Масштабирование спектров давления на стенке после стенозов при установившемся потоке через трубку
. J. Biomech. 9 (1976) 633–640.
3. Кларк, К., Измерения турбулентной скорости в модели стеноза аорты.J. Biomech. 9 (1976)
677–687.
4. Кларк, К., Измерение турбулентного давления стенки в модели стеноза аорты. J. Biomech. 10
(1977) 461–472.
5. Халифа А.М. и Гидденс, Д.П., Анализ нарушений пульсовых потоков с применением к
постстенотическому измерению скорости кровотока у собак. J. Biomech. 11 (1978) 129–141.
6. Гослинг, Р.Г. и King, D.H., Непрерывное ультразвуковое исследование в качестве альтернативы и дополнения
к рентгеновским лучам при обследовании сосудов.В: Ренеман, Р. (ред.), Сердечно-сосудистые применения
ультразвука. Эльзевир, Нью-Йорк (1974), стр. 266–282.
7. Фитцджеральд, Д.Э. и Карр Дж. Ультразвуковая допплеровская диагностика и классификация как альтернатива артериографии
. Ангиология 26 (1975) 283–288.
8. Lees, R.S. и Дьюи, К.Ф., младший, Фоноангиография: новый неинвазивный диагностический метод для
, изучающий артериальные заболевания. Proc. Nat. Акад. Sci. 67 (1970) 935–942.
9. Фредберг, Дж.Дж. Генерация псевдозвука при атеросклеротических сужениях артерий. Бык. Математика.
Биол. 36 (1974) 143–155.
10. Фредберг, Дж. Дж., Происхождение и характер сосудистых шумов: модельные исследования. J. Acoust. Soc. Амер.
61 (1977) 1077–1085.
11. Дункан, Г.В., Грубер, Дж. О., Дьюи, К.Ф., младший, Майерс, Г.С. и Лис, Р.С., Оценка стеноза сонной артерии
с помощью фоноангиографии. NewEng.J.Med.293 (1975) 1124–1128.
12. Питтс, У.Х., III и Дьюи, К.Ф., мл., Спектрально-временные характеристики постстенотических
турбулентных колебаний давления стенки. ASME J. Biomech. Engrg. 101 (1979) 89–95.
13. Гавриэли Н., Палто Ю. и Алрой Г. Спектральные характеристики нормальных звуков дыхания. J. Appl.
Physiol. 50 (1980) 307–314.
14. Краман С.С. Определение места производства дыхательных звуков вычитанием
фонопневмография. Амер. Rev. Resp. Дис. 122 (1980) 303–314.
15.Шарбонне, Дж., Ракцине, Дж. Л., Субро, М. и Туше, Э., Система точной регистрации
и ее использование в спектральном анализе дыхательных звуков. J. Appl. Physiol. 55 (1983) 1120–1127.
16. Коэн А. и Ландсберг Д. Анализ и автоматическая классификация звуков дыхания. IEEE
Пер. Биомед. Engrg. БМЕ-31 (1984) 585–590.
17. Вовк И.В., Гринченко В.Т., Красный Л.Г. и Макаренков А.П. Звуки дыхания: Запись
и задачи классификации.Акуст. Журн. 40 (1994) 50–56.
18. Макаренков А.П., Рудницкий А.

 Не выявлены ключевые гены, ответственные за развитие патологии, точный характер наследования и другие детали.
Не выявлены ключевые гены, ответственные за развитие патологии, точный характер наследования и другие детали. Возникает существенный дефицит тканей. Рост тубулярной груди возможен только по направлению к соску, это приводит к резкому расширению сосково-ареолярного комплекса и развитию ареолярной грыжи.
Возникает существенный дефицит тканей. Рост тубулярной груди возможен только по направлению к соску, это приводит к резкому расширению сосково-ареолярного комплекса и развитию ареолярной грыжи.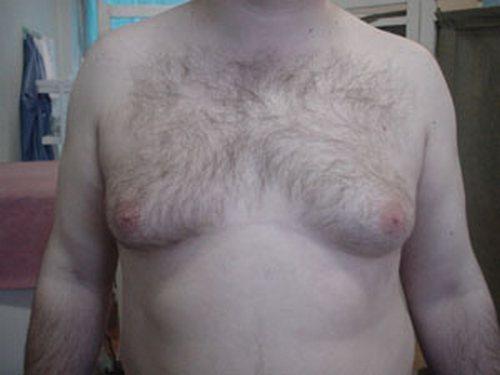 Для равномерного распределения паренхимы железы на ее ткань наносят насечки. В некоторых случаях требуется подбор специальных имплантатов для формирования симметричной груди.
Для равномерного распределения паренхимы железы на ее ткань наносят насечки. В некоторых случаях требуется подбор специальных имплантатов для формирования симметричной груди. По их мнению, патология возникает из-за нарушения кровоснабжения тканей молочных желез, обусловленного заболеваниями, ношением неподходящих бюстгальтеров и пр.
По их мнению, патология возникает из-за нарушения кровоснабжения тканей молочных желез, обусловленного заболеваниями, ношением неподходящих бюстгальтеров и пр. Дефект выражен слабо, молочная железа несколько приподнята вверх, ареола и сосок не изменены. Патология часто не требует коррекции.
Дефект выражен слабо, молочная железа несколько приподнята вверх, ареола и сосок не изменены. Патология часто не требует коррекции. Длительность растяжения составляет не менее 2-3 месяцев в зависимости от выраженности недостатка тканей.
Длительность растяжения составляет не менее 2-3 месяцев в зависимости от выраженности недостатка тканей.