Методы общей анестезии, основанные на закиси азота (веселящем газе), против методов общей анестезии без закиси азота
Вопрос обзора
Мы проанализировали доказательства о вредном влиянии закиси азота на людей, которым проводится общая анестезия (наркоз).
Актуальность
Закись азота является анестезирующим газом, который более 160 лет используется для индукции анестезии и поддержания наркоза на протяжении всей операции. Он также известен как «веселящий газ». Это бесцветный негорючий газ с приятным, слегка сладковатым запахом и вкусом. Его дешевизна и низкая токсичность сделали закись азота на сегодняшний день наиболее часто используемым средством для общей анестезии (наркоза). Однако, некоторые исследования показали, что добавление оксида азота может привести к пагубным последствиям. Это побудило многих анестезиологов задаться вопросом о его дальнейшем рутинном использовании в различных операционных условиях.
Мы хотели выяснить, действительно ли использование закиси азота для общей анестезии было лучше или хуже, нежели его неиспользование.
Характеристика исследований
Мы изучили доказательства, имеющиеся к 17 октября 2014 года. Мы включили 35 испытаний с общим числом 13,872 взрослых участников, которые были рандомизированы в группы, получающие закись азота или не получающие закись азота. Испытания охватывали различные ситуации во время общей анестезии.
Основные результаты
Мы обнаружили, что общая анестезия с закисью азота повышала риск ателектаза легких (т.е. неспособность легких полностью расправиться). Когда мы ограничили результаты только результатами из исследований самого высокого качества, мы обнаружили, что закись азота может потенциально увеличить риск развития пневмонии, тяжелой тошноты и рвоты. Однако, закись азота не оказывала никакого влияния на выживаемость пациентов, частоту инфаркта миокарда, инсульта, раневой инфекции, возникновения тромбов в венах, продолжительности пребывания в стационаре, или длительности пребывания в отделении интенсивной терапии.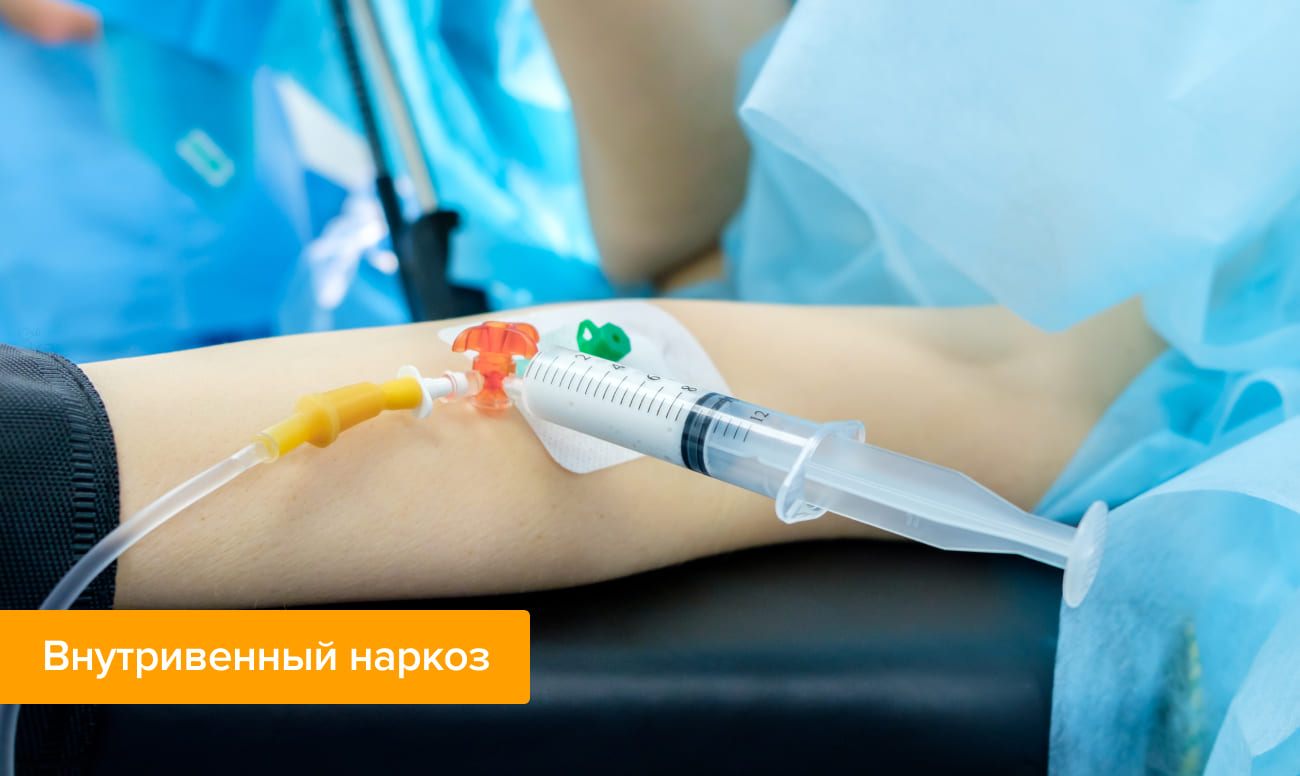
Качество доказательств
Доказательства, связанные с выживанием участников, были среднего качества, так как у нас не было достаточно данных. Доказательства, связанные с некоторыми вредными эффектами: неспособность легких полностью расправиться и сердечные приступы, были высокого качества, в то время как для других вредных эффектов, таких как инсульт и возникновение тромбов в венах, доказательства были среднего качества. Для других исходов, таких как пневмония, тяжелая тошнота и рвота, и раневая инфекция, доказательства были низкого качества. Доказательства, связанные с длительным пребыванием в больнице, были среднего качества.
Отказ от закиси азота может быть разумным для участников с уже существующей недостаточной функцией легких или с высоким риском послеоперационной тошноты и рвоты.
Эпидуральная анестезия | РОСТОВСКАЯ ОБЛАСТНАЯ КЛИНИЧЕСКАЯ БОЛЬНИЦА
Эпидуральная анестезия — это метод обезболивания для проведения хирургического вмешательства путем введения соответствующих препаратов непосредственно в эпидуральное пространство позвоночного столба через катетер. В ходе такого обезболивания также удается добиться расслабления мышц. Эпидуральный наркоз груди, паховой области, ног и живота менее рискован, чем области шеи и рук, а применение такой анестезии для головы в принципе невозможно.
В ходе такого обезболивания также удается добиться расслабления мышц. Эпидуральный наркоз груди, паховой области, ног и живота менее рискован, чем области шеи и рук, а применение такой анестезии для головы в принципе невозможно.
Эпидуральная анестезия также может использоваться:
- в качестве местного обезболивающего средства, если не предполагается хирургическое вмешательство, например, во время родовой деятельности;
- как дополнение к общей анестезии, чтобы снизить количество используемых опиоидов;
- в послеоперационный период для снятия болевого синдрома;
- для терапии болей в спине (в этом случае в эпидуральную область вводятся стероидные препараты и анальгетики).
Когда перед врачом-анестезиологом стоит выбор: общий или эпидуральный наркоз, то при возможности отдается предпочтение последнему. Большой выбор лекарств для его проведения позволяет подобрать для каждого пациента наиболее подходящий вариант, имеются и такие препараты, которые отлично купируют болевой синдром, но сохраняют подвижность и ясность сознания.
Эпидуральная анестезия считается наиболее подходящей для проведения операций на ногах. Она позволяет не только снять болевой синдром и максимально расслабить мышцы, но и снизить кровопотерю. Широко используется во время оперативного вмешательства на органах брюшной полости и малого таза.
Метод доказал свою безопасность для почек и предстательной железы. Сердечно-сосудистая система работает стабильно, так как препарат действует постепенно, его можно использовать при пороках сердца, а также сахарном диабете. Нет раздражения верхних дыхательных путей, как при общем наркозе, что особенно предпочтительно для больных астмой. Однако это не означает, что при таких патологиях всегда применяется эпидуральная анестезия. Решение в каждом конкретном случае принимает врач-анестезиолог строго индивидуально.
Среди абсолютных противопоказаний для применения эпидурального наркоза:
- туберкулезный спондилит или его осложнения;
- воспалительный процесс на спине;
- шоковое состояние в результате травмы;
- повышенная чувствительность к используемым препаратам;
- патология нервной системы;
- деформация позвоночника;
- нарушение процесса свертываемости крови;
- некоторые заболевания брюшной полости;
- кишечная непроходимость.

Также проблемой может стать лишний вес, гипотония, некоторые заболевания неврологического характера. Как правило, эпидуральная анестезия не применяется в детском возрасте.
Качество проведения эпидурального наркоза зависит не только от состояния здоровья пациента, но и от препарата, который используется, и от квалификации врача-анестезиолога — эпидуральный метод обезболивания считается одним из наиболее сложных. Ошибка анестезиолога при введении препарата, когда лекарство попадает внутрь сосуда, может привести к судорогам, резкому снижению артериального давления, есть опасность субарахноидального введения, в результате которого развивается тотальный спинальный блок. Однако при грамотном проведении осложнения в результате эпидуральной анестезии встречаются крайне редко.
МЕХАНИЗМЫ НАРКОЗА | Наука и жизнь
Наркоз — одно из величайших достижений медицины, благодаря которому стала возможна победа над болью в ходе хирургического вмешательства. Без анестезии развитие хирургии до современного уровня было бы просто невозможным.
На картине американского художника Р. Хинкли изображена первая публичная операция под эфирным наркозом.
Этот регулятор подачи эфира, изобретенный Луи Обреденом, применяли вплоть до 70-х годов XX века. На дыхательной маске закреплен тонкостенный металлический шар, внутри которого находятся пропитанные эфиром кусочки фетра.
В XIX веке часто применяли хлороформную маску, сконструированную немецким врачом Куртом Шиммельбушем. С помощью специального держателя на лицо пациента накладывали компресс — пропитанную хлороформом ткань.
‹
›
ПЕРВЫЕ ПОПЫТКИ
До середины XIX века никакого наркоза не знали и даже не предполагали, что когда-нибудь станет возможным оперировать так, чтобы больному было безопасно и небольно, а врачу удобно. И вдруг открытия посыпались одно за другим, как спелые груши под ветром. Видимо, и открытия созрели, и ветер новых идей был силен. Сейчас даже невозможно установить, кто, собственно, был первооткрывателем.
И вдруг открытия посыпались одно за другим, как спелые груши под ветром. Видимо, и открытия созрели, и ветер новых идей был силен. Сейчас даже невозможно установить, кто, собственно, был первооткрывателем.
Официальной датой начала «наркозной эры» считается 16 октября 1846 года, когда американский врач Джон Уоррен впервые оперировал больного под эфирным наркозом. Изобретателями наркоза признаны Уильям Мортон, по профессии зубной врач, и его учитель, врач и химик Чарльз Джексон, который и предложил использовать эфир. Однако еще в 1780 году английский химик Хэмфри Дэви, производя испытания закиси азота на себе, написал: «Закись азота, по-видимому, обладает свойствами уничтожать боль». Но на его слова никто не обратил внимания. Зубной врач из Коннектикута (США) Хорас Уэлс попросил своего коллегу Джона Риггса удалить ему больной зуб во время действия закиси азота, что и было сделано в 1844 году. Боли он не почувствовал, что подтолкнуло Уэлса к применению закиси азота в своей практике.
С эфиром, кстати, тоже не «все чисто». Описание его получения путем перегонки смеси серной кислоты с винным спиртом дал еще в XVI веке немецкий ботаник и аптекарь Валериус Кордус. Отсюда произошло и первое название вещества — серный эфир (позднее его стали называть диэтиловым эфиром или просто эфиром). В начале XVIII века немецкий врач Фридрих Гофман предложил смесь эфира со спиртом в качестве успокаивающих капель, названных его именем; их применяли более ста лет. Чистый эфир был получен лишь в 1796 году Товием Ловицем, работавшим в Главной аптеке в Петербурге. Наркотизирующее действие эфира открыл, как это ни странно, английский физик Майкл Фарадей, который в 1818 году даже опубликовал статью на эту тему.
Умная мысль, как известно, никогда не приходит в единственную голову. Одновременно и независимо друг от друга немецкий химик Юстус Либих и французский аптекарь Эжен Суберан получили новое летучее вещество, которое назвали хлороформом. Никто из них о его наркотизирующем действии не знал. Это установил профессор акушерства Эдинбургского университета Джеймс Симпсон. Не удовлетворенный действием эфира при обезболивании родов, он стал пробовать разные летучие жидкости и, естественно, наткнулся на хлороформ. Уже 15 ноября 1847 хлороформ был применен на практике.
Никто из них о его наркотизирующем действии не знал. Это установил профессор акушерства Эдинбургского университета Джеймс Симпсон. Не удовлетворенный действием эфира при обезболивании родов, он стал пробовать разные летучие жидкости и, естественно, наткнулся на хлороформ. Уже 15 ноября 1847 хлороформ был применен на практике.
Далее началась настоящая гонка за новыми препаратами и новыми методами их применения. Все перечисленные средства были либо газами, либо легко испаряющимися жидкостями, и потому их вводили через дыхательные пути (в то время через простую маску) — ингаляционно, то есть путем вдыхания. Такой метод затруднял операции на лице или в положении больного на животе. Это привело Николая Ивановича Пирогова к попыткам вводить наркотические препараты в прямую кишку, то есть неингаляционно, что, впрочем, имело свои недостатки.
В 1899 году профессор Генрих Дрезер сообщил о создании нового активного снотворного — гедонала, производного уретана. Используя это снотворное, профессор Военно-медицинской академии Николай Павлович Кравков разработал способ наркотизации с предварительным введением медикамента. Сначала больному давали таблетку гедонала, которая обеспечивала глубокий сон, а на его фоне — хлороформ. При этом и наркотизация протекала спокойней, и хлороформа требовалось меньше.
Сначала больному давали таблетку гедонала, которая обеспечивала глубокий сон, а на его фоне — хлороформ. При этом и наркотизация протекала спокойней, и хлороформа требовалось меньше.
Позднее было предложено введение одного гедонала внутривенно. Первая операция с применением внутривенного наркоза выполнена в 1909 году в клинике Сергея Петровича Федорова в Петербурге. Неингаляционный гедоналовый наркоз, который назвали «русским способом наркоза», стал вытеснять хлороформ. Вскоре, впрочем, он был заменен гексеналом, производным барбитуратов (к ним относится, в частности, фенобарбитал). Химические формулы упомянутых первых средств, использованных для наркоза, чрезвычайно отличаются одна от другой, хотя и вызывают почти одинаковый эффект. Добавим, что наркоз можно вызвать и электротоком и гипнозом.
ЧТО ЖЕ ТАКОЕ НАРКОЗ?
Слово «наркоз» происходит от греческого narke, что значит оцепенение, онемение. Согласно учебнику по фармакологии, это состояние, характеризующееся обратимым угнетением центральной нервной системы, проявляется выключением сознания, подавлением чувствительности (в первую очередь болевой), рефлекторных реакций и снижением тонуса мышц.
Такое определение описывает лишь внешнюю картину, но не дает характеристики наркоза и не вскрывает механизм его возникновения. Начать с того, что несведущий человек затруднится отличить состояние наркоза от сотрясения мозга, солнечного удара и даже обморока. Потеря сознания происходит во время простого сна, не говоря уже о коме (греч. koma — глубокий сон) любого происхождения. Конечно, при всех этих состояниях потеря сознания сопровождается нарушением функции жизненно важных органов и систем. При наркозе такого быть не должно, и это надо бы оговорить в определении. Кроме того, кома может возникнуть как результат передозировки наркотизирующего средства, следовательно, речь в определении идет не о наркозе вообще, а об относительно безопасном хирургическом наркозе.
Наркоз без потери сознания — рауш-наркоз, предложенный, кстати, Н. И. Пироговым, — самая первая стадия наркоза, при которой устраняется только чувствительность, что достаточно для проведения мелких операций.
Сравнительно недавно увлекались так называемым «наркозом без наркоза», по медицинской терминологии — нейролептаналгезией. Больному вводили сильный нейролептик дроперидол, который устраняет передачу нежелательных рефлексов с оперируемого органа на другие органы и системы, предупреждает шок, а плюс к тому подавляет страх, напряжение, рвоту и усиливает действие и без того мощного анестетика фентанила. При этом больной не теряет сознание.
Больному вводили сильный нейролептик дроперидол, который устраняет передачу нежелательных рефлексов с оперируемого органа на другие органы и системы, предупреждает шок, а плюс к тому подавляет страх, напряжение, рвоту и усиливает действие и без того мощного анестетика фентанила. При этом больной не теряет сознание.
С другой стороны, барбитураты, используемые и сейчас для неингаляционного наркоза, например гексенал и тиопентал, не подавляют чувства боли, то есть не являются анестетиками! Оказывается, простого глубокого сна может быть достаточно для выполнения операции.
Именно поэтому такие сильные снотворные теперь называют гипнотиками. В американской литературе указывается, что при тиопенталовом наркозе 10 процентов оперируемых чувствуют боль, что неоднократно становилось причиной судебных исков. Все же этот факт дает понять, почему при гипнозе можно оперировать вообще без химического вмешательства. Теперь имеются прекрасные анестетики, которые не расслабляют мускулатуру, например кетамин.
Для выполнения некоторых операций приходится дополнительно вводить вещества, которые только расслаблением мышц и занимаются, — миорелаксанты. Но не всегда оно нужно, это расслабление. Вот поэтому сейчас от термина «наркоз» уже практически отказались. Теперь говорят «общая анестезия». Да оно и удобней: легче различать общую анестезию от местной, для достижения которой используются совсем другие вещества — местные анестетики типа новокаина, лидокаина и им подобных.
Этот регулятор подачи эфира, изобретенный Луи Обреденом, применяли вплоть до 70-х годов XX века. На дыхательной маске закреплен тонкостенный металлический шар, внутри которого находятся пропитанные эфиром кусочки фетра. Выдыхаемый пациентом воздух собирается в пакете. С помощью специального устройства можно регулировать подачу эфира, свежего воздуха и обратное вдыхание из пакета.
Действительно, для операции главное — устранить все ощущения, а сон любой глубины, подавление рефлексов и расслабление мышц можно вызвать при необходимости другими веществами. Так что хирургический наркоз — это общая анестезия в сочетании с гипнотиками, транквилизаторами, нейролептиками, веществами, блокирующими патологические рефлексы, и миорелаксантами, благодаря чему удается получить полностью безопасное и лишенное неприятных ощущений состояние, которое обеспечивает хирургу возможность произвести необходимое вмешательство.
Так что хирургический наркоз — это общая анестезия в сочетании с гипнотиками, транквилизаторами, нейролептиками, веществами, блокирующими патологические рефлексы, и миорелаксантами, благодаря чему удается получить полностью безопасное и лишенное неприятных ощущений состояние, которое обеспечивает хирургу возможность произвести необходимое вмешательство.
Но почему же многие вещества, такие разные, способны приводить человека в состояние, сходное с типичным хирургическим наркозом? Наркоз, вызываемый кетамином или эфиром, не может обеспечиваться тем же механизмом, что и наркоз после введения инертного газа ксенона или тем более гипнотического внушения. Тут идут одни предположения.
СКОЛЬКО ВЕЩЕСТВ, СТОЛЬКО ТЕОРИЙ?
Мозг — чудесное скопление нервных клеток числом порядка 1010, то есть десять миллиардов штук. Все они имеют по нескольку отростков, которые вроде бы переплетаются, но на самом деле нигде не соприкасаются. Импульсы по отросткам передаются при помощи электричества, но оно выполняет лишь роль спускового крючка. Нервное окончание, получив удар током, выстреливает мелкими молекулами передатчиков-медиаторов, которые, войдя в соприкосновение с клеткой-мишенью, меняют ее состояние. Она либо возбуждается, либо тормозится, либо полностью теряет чувствительность, замирает.
Нервное окончание, получив удар током, выстреливает мелкими молекулами передатчиков-медиаторов, которые, войдя в соприкосновение с клеткой-мишенью, меняют ее состояние. Она либо возбуждается, либо тормозится, либо полностью теряет чувствительность, замирает.
Первая теория, объясняющая действие наркотизирующих веществ, создана в 1875 году французским физиологом Клодом Бернаром и названа коагуляционной. Было отмечено, что под действием эфира и хлороформа происходит обратимая коагуляция (свертывание) внутриклеточных белков в изолированных нейронах. Однако в 1938 году русский хирург П. И. Макаров доказал, что при прижизненном наблюдении за клетками во время хлороформного наркоза никакой коагуляции не происходит — концентрация наркотика для этого слишком мала.
Следующая теория Э. Овертона и Г. Мейера, созданная в 1899 году, названа липидной. Предполагалось, что наркотические вещества действуют тем сильнее, чем лучше растворяются в липидах (жирах). Но после получения новых веществ, в частности гексенала и тиопентала, а также стероидных анестетиков (виадрил и другие), которые плохо растворимы в жирах, а действуют сильно, эта теория сохранилась лишь в той части, что вообще-то наркотики должны в какой-то мере действительно быть жирорастворимыми. Оно и понятно, совсем не растворимые в жирах вещества не могут ни пройти сквозь гематоэнцефалический барьер мозга, ни проникнуть внутрь клетки через клеточную мембрану.
Оно и понятно, совсем не растворимые в жирах вещества не могут ни пройти сквозь гематоэнцефалический барьер мозга, ни проникнуть внутрь клетки через клеточную мембрану.
Пересказывать все теории в исторической последовательности нет смысла. Их было много — протеиновая, теория изменения поверхностного натяжения мембран, термодинамическая, теория образования водных кристаллов, теория нарушения окислительных процессов, — но все они давали лишь частичное объяснение для какой-то группы веществ. В настоящее время наиболее популярна мембранная теория. Согласно этой теории, включение молекул наркотизирующего вещества в мембрану клеток затрудняет проникновение через нее активных ионов, в частности натрия, калия и кальция, осуществляющих генерацию электрических потенциалов действия. В результате электроактивность нейронов нарушается. Поскольку большинство наркотических веществ химически инертно, то предполагается, что они вступают с мембраной не столько в химическое, сколько в физическое взаимодействие.
УНИВЕРСАЛЬНЫЙ ТОРМОЗ
А теперь еще одна неожиданность. В 1950 году американские химики У. Робертс и С. Френкель обнаружили в мозге новую аминокислоту, которую они назвали гамма-аминомасляной кислотой (ГАМК). Было странно, что эта кислота не встраивается в белки, а находится как бы в свободном плавании. Зачем? Ответ получили через десять с небольшим лет. Английский ученый К. Крньевич подвел слабый раствор ГАМК к одной из корковых клеток, воспринимающих чувствительные импульсы. Каково же было его удивление, а затем и восторг, когда он установил, что ГАМК подавила реактивность чувствительных клеток коры мозга, то есть является тормозным веществом. Японские авторы сделали еще проще. К чувствительной зоне коры они подвели плавающий электрод, а на него сверху надели бумажку, смоченную ГАМК. Тот же результат. Японский опыт позднее был воспроизведен автором этой статьи.
Потом обнаружили , что ГАМК тормозит не только клетки, воспринимающие импульсы, но и клетки, их генерирующие. Дальше — больше. И вот наконец установили, что это вещество является тормозным медиатором примерно для 20-30 процентов нервных клеток. Были составлены карты действия ГАМК в мозге, причем они совпали с теми зонами, которые ответственны за сон и боль.
Дальше — больше. И вот наконец установили, что это вещество является тормозным медиатором примерно для 20-30 процентов нервных клеток. Были составлены карты действия ГАМК в мозге, причем они совпали с теми зонами, которые ответственны за сон и боль.
Мало того, при окислении ГАМК образуется оксибутират, который оказался наркотизирующим средством, хотя и слабым. Так было доказано, что наркоз может быть не только мембранным, но и синаптическим, а именно — вызывать эффект в результате химической реакции с теми участками клеток-испол нительниц, которые подчиняются специальным химическим командам.
Кстати, вещества бензодиазепиновой группы и барбитураты оказывают центральное успокаивающее, противосудорожное и расслабляющее мышцы действие, активируя рецепторы, чувствительные к ГАМК.
Логично было бы предположить, что в противовес универсальному тормозному фактору должен существовать и универсальный активирующий фактор. Действительно, таковым оказалась известная с 1866 года и широко распространенная в организме, в том числе и в мозге, глутаминовая кислота, а также ее амид — глутамат. В 1974 году Д. Куртис и Г. Джонстон (США) установили, что при воздействии глутамата на молчащие нервные клетки в них возникает активность, что и позволило отнести глутаминовую кислоту к возбуждающим аминокислотам.
В 1974 году Д. Куртис и Г. Джонстон (США) установили, что при воздействии глутамата на молчащие нервные клетки в них возникает активность, что и позволило отнести глутаминовую кислоту к возбуждающим аминокислотам.
В XIX веке часто применяли хлороформную маску, сконструированную немецким врачом Куртом Шиммельбушем. С помощью специального держателя на лицо пациента накладывали компресс — пропитанную хлороформом ткань. Чтобы действие наркоза не ослабевало, время от времени ткань дополнительно смачивали хлороформом. Наибольшая опасность состояла в передозировке и блокаде дыхательных путей.
Примерно в те же годы в нашей стране был введен в практику новый неингаляционный общий анестетик кетамин (кеталар, калипсол). Кетамин обладает выраженным анальгетическим эффектом благодаря химической активации опиатных рецепторов мозга; при этом из депо высвобождаются эндогенные анальгетики — энкефалины. Особый интерес представляет способность кетамина блокировать некоторые рецепторы глутамата, снижая таким образом как общую активность мозга, так и опосредуемое через них восприятие боли.
Итак, окончательного, тем более универсального ответа на вопрос о механизме действия веществ, вызывающих наркоз, нет. Предварительно можно сказать, что общие анестетики могут быть разделены на две группы: вещества, взаимодействующие с мембранами нейронов за счет своих физических свойств, и вещества, оказывающие избирательное химическое действие на определенные клеточные рецепторы, участвующие в формировании ощущения боли.
Неясностей остается достаточно. Так и не решен вопрос о том, каким же образом столь разнообразные вещества и воздействия способны вызывать практически неразличимую картину наркоза. Возможно, что в мозге высших животных сохранилась некая универсальная система, которая у низших организмов участвует в пассивной защитной реакции оцепенения и мнимой смерти. Если это так, то активировать ее способны самые разные стимулы и воздействия на различные отделы мозга. Сказанное нельзя даже рассматривать как гипотезу, только лишь как предположение.
ФЕНТАНИЛ И БОРЬБА С ТЕРРОРИЗМОМ
Во время операции по освобождению заложников, захваченных террористами в октябре 2002 года в Москве, спецслужбы применили фентанил (об этом было заявлено официально). Поскольку анальгетик фентанил применяется как наркотизирующее вещество (о чем упоминалось выше), стоит поговорить о нем подробнее.
Поскольку анальгетик фентанил применяется как наркотизирующее вещество (о чем упоминалось выше), стоит поговорить о нем подробнее.
Вo всех странах, помимо боевых отравляющих веществ смертельного действия типа зарина, существовали и существуют теоретически несмертельные отравляющие вещества, условно называемые «полицейскими «, которые, разумеется, могут быть использованы и в боевых условиях, а поэтому держатся в полусекрете. На смену слезоточивым газам неминуемо должны были прийти другие. И пришли.
В последние годы в международных научных журналах публиковались статьи о том, что в качестве полицейского оружия (будем именовать его так) могут быть использованы вещества психотропного действия, которые не включены в Конвенцию о запрещении производства и хранения отравляющих веществ. В числе прочих упоминались и производные морфина. Достаточно хорошо известно, что морфин — это не только болеутоляющее, но и наркотическое, а следовательно, психотропное вещество. В терапевтических дозах морфин и синтетические морфиноподобные вещества типа промедола действуют в мозге только на чувствительные к опию (опиоидные) клетки, подавляя боль. Но уже в минимально токсических дозах сам морфин снижает восприятие окружающего, подавляет активность, вызывает безразличие и полусонное состояние — не явь, но и не сон, тем более, не наркоз. Выражаясь образно — обалдение.
Но уже в минимально токсических дозах сам морфин снижает восприятие окружающего, подавляет активность, вызывает безразличие и полусонное состояние — не явь, но и не сон, тем более, не наркоз. Выражаясь образно — обалдение.
При введении токсических доз морфинов возбуждается рвотный центр и угнетается дыхательный центр. По мере синтеза новых веществ дошли и до фентанила, сходного по строению с промедолом, но примерно в 100 раз более активного. На практике оказалось, что фентанил обеспечивает обезболивание достаточное, чтобы произвести хирургическую операцию. Второе его достоинство — быстрота наступления эффекта, от 1 до 5 минут. Недостаток для хирургии заключается в кратковременности действия — 15-30 минут. Для полицейских целей это как раз достоинство. Правда, полицейским хотелось бы, чтобы побочные действия фентанила — одурманивание, спастическое сокращение мышц, рвотный эффект — были более выражены. А вот угнетение дыхательного центра в любом случае является недостатком, поскольку при отсутствии аппарата для искусственного дыхания может обернуться катастрофой.
По-видимому, во время спецоперации в театральном центре использовали одно из производных фентанила, возможно диметилфентанил. Хотя это вещество не приводит к гибели здоровых взрослых людей, но, как все опиоиды, оно опасно для детей, для больных бронхиальной астмой, диабетом и для тех, кто находится в состоянии сильного стресса. А таковых среди заложников было много. Именно это, а также недостаточная подготовленность медицинских служб для оказания помощи большому количеству пострадавших стали причиной гибели людей.
Да, большинство токсических эффектов как самого морфина, так и синтетических опиоидов устраняется их антагонистами — налорфином и налоксоном, однако угнетения дыхания они не снимают, а обеспечить всех аппаратами для принудительной вентиляции легких было нереально.
Есть и еще один момент. Дело в том, что все синтетические опиоиды, начиная с фентанила, — порошки или их растворы. Но не будешь же бегать за каждым террористом со шприцем! Однако еще на заре появления первых ядов типа ДЛК (диэтиламид никотиновой кислоты), вызывающих психозоподобные состояния, были сконструированы специальные аэрозольные генераторы, позволяющие создавать целые облака, включающие твердые частицы столь малых размеров, что они не задерживаются даже стандартными противогазами. Для успеха операции в театральном центре требовалось очень быстро насытить аэрозолем зрительный зал, что и было сделано. Гораздо проще применять этот метод в небольших закрытых помещениях. Не скрою, меня удивляло, что такие операции до настоящего времени не предпринимались при освобождении заложников в самолетах.
Для успеха операции в театральном центре требовалось очень быстро насытить аэрозолем зрительный зал, что и было сделано. Гораздо проще применять этот метод в небольших закрытых помещениях. Не скрою, меня удивляло, что такие операции до настоящего времени не предпринимались при освобождении заложников в самолетах.
См. в номере на ту же тему
статья РЫЖЕВОЛОСЫЕ СИЛЬНЕЕ ЧУВСТВУЮТ БОЛЬ
Как действует анестезия? — Scientific American
Объясняет Билл Перкинс, доцент анестезиологии медицинского колледжа Мэйо в Рочестере, штат Миннесота. Оливер Венделл Холмс ввел термин «анестезия» в 1846 году для описания нечувствительности к ощущениям (особенно боли), вызванной лекарствами, вскоре после того, как первая публичная демонстрация вдыхаемого эфира сделала пациента невосприимчивым во время хирургической процедуры. Два широких класса фармакологических агентов, местные и общие, могут привести к анестезии.Местные анестетики, такие как новокаин, блокируют нервную передачу к болевым центрам в центральной нервной системе, связываясь и подавляя функцию ионного канала в клеточной мембране нервных клеток, известного как натриевой канал. Это действие препятствует движению нервных импульсов рядом с местом инъекции, но не происходит никаких изменений в осознании и чувственном восприятии в других областях.
Это действие препятствует движению нервных импульсов рядом с местом инъекции, но не происходит никаких изменений в осознании и чувственном восприятии в других областях.
Напротив, общие анестетики вызывают анестезирующее состояние другого типа, а именно общую нечувствительность к боли.Пациент теряет сознание, но его жизненно важные физиологические функции, такие как дыхание и поддержание артериального давления, продолжают функционировать. О механизме действия общих анестетиков известно меньше, чем у местных, несмотря на то, что они используются более 150 лет. Наиболее часто используемые общие анестетики вводятся путем дыхания и поэтому называются ингаляционными или летучими анестетиками. Они структурно связаны с эфиром, исходным анестетиком. Их основное действие находится в центральной нервной системе, где они подавляют нервную передачу по механизму, отличному от местного анестетика.Общие анестетики вызывают снижение нервной передачи в синапсах, местах, в которых нейротрансмиттеры высвобождаются и проявляют свое первоначальное действие в организме. Но как именно ингаляционные анестетики подавляют синаптическую нейротрансмиссию, еще полностью не изучено. Однако ясно, что летучие анестетики, которые более растворимы в липидах, чем в воде, в первую очередь влияют на функцию ионных каналов и белков рецепторов нейротрансмиттеров в мембранах нервных клеток, которые представляют собой липидную среду.
Но как именно ингаляционные анестетики подавляют синаптическую нейротрансмиссию, еще полностью не изучено. Однако ясно, что летучие анестетики, которые более растворимы в липидах, чем в воде, в первую очередь влияют на функцию ионных каналов и белков рецепторов нейротрансмиттеров в мембранах нервных клеток, которые представляют собой липидную среду.
Два фактора затрудняют получение подробного описания того, как действуют эти агенты. Во-первых, летучие анестетики, в отличие от большинства лекарств, используемых в медицине, очень слабо связываются с местом (ами) своего действия. В результате для достижения анестезирующего состояния необходимы высокие концентрации, часто более чем в 1000 раз превышающие обычные рецепторы или нацеленные на белок лекарственные средства. Это затрудняет получение структурных деталей анестетиков, связанных особым образом с белком.Он также влияет на функцию многих белков в мембранах нервных клеток, что затрудняет определение того, какие из них являются ключевыми медиаторами анестезирующего действия. Вторая проблема заключается в том, что летучие анестетики имеют тенденцию разделяться на липиды и оказывать свое основное влияние на синаптическую нейротрансмиссию, взаимодействуя с белками в липидной среде. Для мембранных белков сложнее получить подробную структурную информацию, чем для водорастворимых белков. Такие структурные данные необходимы для понимания того, как анестетики взаимодействуют с белками и, что более важно, изменяют их функцию.Из-за отсутствия структурных данных для мембранных белков как в присутствии, так и в отсутствие анестетиков остается неясным, оказывают ли анестетики свои основные эффекты путем прямого взаимодействия с этими белками или косвенно через взаимодействие с окружающими их липидами.
Вторая проблема заключается в том, что летучие анестетики имеют тенденцию разделяться на липиды и оказывать свое основное влияние на синаптическую нейротрансмиссию, взаимодействуя с белками в липидной среде. Для мембранных белков сложнее получить подробную структурную информацию, чем для водорастворимых белков. Такие структурные данные необходимы для понимания того, как анестетики взаимодействуют с белками и, что более важно, изменяют их функцию.Из-за отсутствия структурных данных для мембранных белков как в присутствии, так и в отсутствие анестетиков остается неясным, оказывают ли анестетики свои основные эффекты путем прямого взаимодействия с этими белками или косвенно через взаимодействие с окружающими их липидами.
Несмотря на эти ограничения, исследователи используют различные методы, чтобы лучше понять, как анестетики вызывают анестезирующее «состояние» на молекулярном уровне. Термин «состояние» заключен в кавычки, потому что широкий спектр агентов — от отдельных атомов, таких как ксенон, до полициклических углеводородов — может вызывать нечувствительность к боли и потерю сознания. Молекулярные мишени для этих разных агентов не одинаковы. Таким образом, представление о том, что существует единый молекулярный механизм действия всех анестетиков, вероятно, является чрезмерным упрощением.
Молекулярные мишени для этих разных агентов не одинаковы. Таким образом, представление о том, что существует единый молекулярный механизм действия всех анестетиков, вероятно, является чрезмерным упрощением.
Генетические инструменты дают многообещающие результаты в отношении молекулярного механизма анестезирующего действия. Например, исследователи могут изменить конкретную функцию белка, а затем определить, может ли этот белок быть связан с чувствительностью или устойчивостью к анестезирующему действию у низших организмов.Эти подходы определяют, какие белки участвуют в анестезиологическом действии, и могут рассматриваться как способ более точного определения соответствующих целей анестетика, на которых исследователи могут затем сосредоточиться для структурных исследований. Другие подходы, включая сложное структурное моделирование связывания анестетика с белками-мишенями в липидной среде и подробные структурные определения связывания анестетика с растворимыми белками, также демонстрируют многообещающие перспективы в дальнейшем раскрытии того, как анестетик действует на молекулярном уровне.
Таким образом, простой ответ на вопрос «Как действует анестезия?» заключается в том, что, хотя мы много знаем о физиологических эффектах и макроскопических участках действия, мы еще не знаем молекулярный механизм (ы) действия общих анестетиков. Сейчас существует множество инструментов, необходимых для ответа на эти вопросы, и мы можем надеяться на новое понимание того, как это великое благо для человечества работает на молекулярном уровне.
Как работает анестезия? Объяснение эксперта
Современные медицинские технологии и методы лечения настолько распространены, что мы часто не задумываемся о них дважды.Рентген, ультразвук и аппендэктомия просто стали реальностью. Такие достижения медицины легко принять как должное. Но без них было бы намного труднее оставаться в безопасности и здоровьем.
Задумайтесь на минутку, как нам повезло, что у нас есть доступ к анестезии. Без него невозможно было бы сделать многие рутинные операции.
Хотя у вас, вероятно, есть смутное представление об анестезии, у вас, вероятно, есть некоторые вопросы. Что именно? А как действует анестезия? Взгляните на этот обзор, чтобы узнать.
Что такое анестезия?
В простейшем смысле анестезия — это лекарство, которое помогает облегчить боль или дискомфорт во время процедуры. Существует множество видов и способов доставки. Кроме того, в зависимости от пациента и процедуры можно использовать разные препараты в комбинациях.
Доктор Эдна Ма, анестезиолог, практикующий в хирургическом медицинском центре
, добавляет, что анестезия состоит из трех основных компонентов.Их можно использовать вместе или по отдельности. Это следующие компоненты:
• Обезболивание — уменьшение или устранение боли
• Амнезия — временная и может включать потерю сознания
• Расслабление мышц
Хотя вы уже знаете, что анестезия используется во время серьезных операций, это не единственное применение. Его также применяют для неинвазивных процедур, которые в противном случае могут быть неудобными. Доктор Ма говорит, что анестезию можно использовать при получении магнитно-резонансной томографии (МРТ), например, у ребенка или пациента, страдающего клаустрофобией.
Его также применяют для неинвазивных процедур, которые в противном случае могут быть неудобными. Доктор Ма говорит, что анестезию можно использовать при получении магнитно-резонансной томографии (МРТ), например, у ребенка или пациента, страдающего клаустрофобией.
«Практически неподвижный пациент имеет решающее значение для получения оптимальных изображений МРТ».
«Практически неподвижный пациент имеет решающее значение для получения оптимальных изображений МРТ», — объясняет она. «Пациент под наркозом будет по существу неподвижен».
Какие бывают виды анестезии?
Хотя существует множество лекарств, которые анестезиологи используют в различных комбинациях, Dr.Ма выделяет четыре основных типа. Каждая из этих категорий используется для разных видов ухода. Это ни в коем случае не исчерпывающее объяснение, но оно должно дать вам представление о том, чего вы можете ожидать, если вам или близкому человеку понадобится процедура.
1. Общая анестезия используется для вывода пациента в бессознательное состояние и применяется при инвазивных операциях, таких как лапароскопическая герниопластика. Доктор Ма также добавляет, что анестезиолог контролирует дыхание пациента.
Общая анестезия используется для вывода пациента в бессознательное состояние и применяется при инвазивных операциях, таких как лапароскопическая герниопластика. Доктор Ма также добавляет, что анестезиолог контролирует дыхание пациента.
2.Седативный наркоз используется для малоинвазивных процедур, таких как колоноскопия. «Это включает легкую или умеренную внутривенную седацию, при которой пациент дышит самостоятельно», — объясняет доктор Ма.
3. Местная анестезия включает инъекцию в место операции, но пациент не спит. Его часто используют, чтобы обезболить область перед наложением швов.
4. Регионарная анестезия обезболивает большую часть тела, пока пациент не спит. Пожалуй, наиболее широко распространена эпидуральная анестезия, которая делает роды более комфортными для женщин.
Как действует анестезия?
На основании приведенной выше информации ясно, что не существует одного конкретного способа действия анестезии. И исследователи действительно только начинают понимать, как действуют различные лекарства, применяемые для обезболивания и обезболивания. Они думают, что лекарства нацелены на различные белки мембран вокруг нервных клеток.
Пропофол — одно из наиболее распространенных лекарств, используемых для общей анестезии.Исследование 2018 года было посвящено пропофолу, чтобы выяснить, какие механизмы действуют. Исследование показало, что этот тип анестезии ограничивает движение определенного типа белка таким образом, что препятствует коммуникации между нейронами. Но авторы исследования также отмечают, что предстоит еще многому научиться.
И помните, разные лекарства дают разные результаты. Вопрос о том, как действует анестезия, еще больше усложняется тем фактом, что разные типы часто необходимо использовать в сочетании друг с другом.Одного лекарства может быть недостаточно для данной процедуры.
«Лекарство, такое как пропофол, может вызвать потерю сознания, но не имеет обезболивающего действия».
«Лекарство, такое как пропофол, может вызвать потерю сознания, но не имеет обезболивающего действия», — отмечает доктор Ма.
Важно, чтобы она знала, что делает каждое лекарство, а также соответствующую комбинацию на каждом этапе процедуры. Анестезия — это не просто щелкнуть выключателем и уйти.Он требует постоянного контроля и настройки, особенно при сложных операциях.
«При проведении анестезии для трепанации черепа в сознании» пациенту необходимо оставаться полностью неподвижным, — говорит доктор Ма. «Однако во время части операции пациенту нужно будет бодрствовать и говорить».
Другой пример, который предлагает доктор Ма, — это операция на плече, когда пациент сидит. Это потребует общей анестезии, а также может быть проведена блокада нерва (региональная анестезия) перед операцией, чтобы минимизировать боль и помочь в процессе восстановления.
Если все это звучит как тщательный баланс, то это потому, что это так. Вот почему любой врач, проводящий анестезию, должен быть хорошо обучен. Эти медицинские специалисты включают анестезиологов, медсестер-анестезиологов, хирургов-стоматологов, стоматологов и ассистентов анестезиологов.
Опасна ли анестезия?
Если вы посмотрите на историю анестезии, нельзя отрицать, что когда-то это была рискованная практика. Только в 1846 году была проведена первая успешная операция с использованием анестезии.Эта область быстро развивалась в 1900-х годах, и теперь анестезия считается обычным делом. Хотя пациенты все еще могут испытывать осложнения, они случаются редко.
«Современная анестезия чрезвычайно безопасна», — подчеркивает доктор Ма. «Общий уровень смертности составляет около 0,03, или 3 смерти на 10 000 операций или процедур с применением анестезии».
«Современная анестезия чрезвычайно безопасна».
Расширьте свои знания в этой области
Как работает анестезия? Вы можете видеть, что это зависит от типа лекарства и оказываемой помощи.Когда врачи определяют лучший план анестезиологической помощи для отдельных пациентов, в игру вступают такие переменные факторы. Возможно, им даже придется скорректировать свои планы во время процедуры.
Хотя это может показаться пугающим, специалисты здравоохранения, которые проводят анестезию, обучены быть готовы ко всему. Особенно это касается анестезиологов. Узнайте больше о том, чем занимаются эти специалисты, прочитав нашу статью « Что такое анестезиолог? Понимание этой роли в хирургической помощи .”
Мы наконец знаем, как работает общая анестезия
Поделиться
Артикул
Вы можете поделиться этой статьей в соответствии с международной лицензией Attribution 4.0.
В новом исследовании исследователи обнаружили, что, чтобы вырубить вас, различные анестезирующие препараты захватывают нервную систему, которая заставляет вас засыпать.
Открытие общей анестезии 170 лет назад стало медицинским чудом, позволив миллионам пациентов безболезненно перенести инвазивные, спасающие жизнь операции.
Лекарства для общей анестезии вызывают бессознательное состояние, активируя крошечный кластер клеток в основании мозга, называемый супраоптическим ядром (показано красным), в то время как остальная часть мозга остается в основном в неактивном состоянии (синий). (Фото: Герцог)В исследовании, которое проводится в Neuron , исследователи проследили эту нейронную схему до крошечного кластера клеток в основании мозга, ответственного за выработку гормонов для регулирования функций организма, настроения и сна.
Это открытие является одним из первых, предполагающих роль гормонов в поддержании состояния общей анестезии, и дает ценную информацию для создания новых лекарств, которые могут усыпить людей с меньшими побочными эффектами.
С тех пор, как первый пациент прошел под общим наркозом в 1846 году, ученые пытались выяснить, как именно это работает. Преобладала теория, что многие из этих препаратов подавляют нормальную деятельность мозга, что приводит к неспособности двигаться или чувствовать боль.
Подобные теории вращались вокруг сна, родственного состояния общей анестезии. Однако исследования последнего десятилетия показали, что сон — более активный процесс, чем считалось ранее, когда целые наборы нейронов работают, пока вы ловите свои Z.
Фань Ван, профессор нейробиологии медицинского факультета Университета Дьюка, и Ли-Фэн Цзян-Се, аспирантка в ее лаборатории, задались вопросом, является ли преобладающее мнение об общей анестезии также односторонним.
«Возможно, вместо того, чтобы просто подавлять нейроны, анестетики также могут активировать определенные нейроны в головном мозге», — говорит Цзян-Се.
Чтобы проверить свою новую теорию, Цзян-Се и Лупин Инь, научный сотрудник лаборатории Ванга, подвергли мышей общей анестезии несколькими различными, но обычно используемыми лекарствами. Затем они использовали молекулярные маркеры, чтобы отследить нейроны, обычно активируемые анестетиками.
Они обнаружили скопление активно возбуждающих нейронов, похороненных в крошечной области мозга, называемой супраоптическим ядром, которое, как известно, имеет длинные выступы, которые выделяют большое количество гормонов, таких как вазопрессин, непосредственно в кровоток.
«Большинство клеток, активируемых анестезией, были своего рода гибридными клетками, соединяющими нервную систему и эндокринную систему», — говорит Цзян-Се. «Это застало нас врасплох и привело к неизведанной территории для понимания нервных путей общей анестезии».
Затем исследователи применили сложную технику, разработанную в лаборатории Ванга, для включения или выключения этой специализированной группы клеток с помощью химических веществ или света. Когда они включали клетки у мышей, животные перестали двигаться и впадали в глубокий сон, называемый медленным сном, обычно связанный с потерей сознания.
Затем группа исследователей уничтожила эту группу клеток. Мыши продолжали передвигаться, не имея возможности заснуть.
Наконец, исследователи провели аналогичные эксперименты на мышах под общим наркозом. Они обнаружили, что искусственная предварительная активация нейроэндокринных клеток заставляла мышей оставаться под общей анестезией в течение более длительных периодов времени. И наоборот, когда они заставили эти клетки замолчать, мыши легче просыпались от анестезии.
Исследование также выявило ранее неожиданную роль клеток мозга, секретирующих гормоны, в обеспечении глубокого сна.
«Многие люди, особенно страдающие болезнью Альцгеймера, испытывают трудности с засыпанием, однако современные лекарства имеют неприятные побочные эффекты», — говорит Инь. «Если мы сможем найти способы манипулировать этой нейронной схемой, возможно, путем нацеливания на гормоны или небольшие пептиды, то это может привести к разработке лучших снотворных».
Фонд В. М. Кека, Фонд исследований мозга, Национальные институты здоровья и научное сообщество Human Frontier Science Fellowship финансировали работу.
Источник: Duke University
Исследование на мозге мышей и крыс показывает, как общая анестезия снижает высокочастотную активность мозга за счет ослабления синапсов — ScienceDaily
Открытие общих анестетиков — соединений, которые вызывают бессознательное состояние и препятствуют контролю над ними, — названо одним из самых важных медицинских достижений. движение и блокирование боли — помогли превратить опасные и травматические операции в безопасные и рутинные операции.Но, несмотря на их важность, ученые до сих пор не понимают, как именно работают общие анестетики.
Итак, в исследовании, опубликованном на этой неделе в журнале Journal of Neuroscience , исследователи из Окинавского института науки и технологий аспирантуры (OIST) и Университета Нагоя показали, как широко используемый общий анестетик, называемый изофлураном, ослабляет передачу электрических сигналов. между нейронами, в соединениях, называемых синапсами.
«Важно отметить, что мы обнаружили, что изофлуран не блокировал передачу всех электрических сигналов в равной степени; анестетик оказал сильнейшее влияние на более высокочастотные импульсы, необходимые для таких функций, как познание или движение, в то время как он оказал минимальное влияние на низкочастотные импульсы, которые контролировать жизненно важные функции, такие как дыхание », — сказал профессор Томоюки Такахаши, возглавляющий Отделение клеточной и молекулярной синаптической функции (CMSF) в OIST.«Это объясняет, как изофлуран может вызывать анестезию, преимущественно блокируя высокочастотные сигналы».
В синапсах сигналы посылаются пресинаптическими нейронами и принимаются постсинаптическими нейронами. В большинстве синапсов общение происходит через химические мессенджеры или нейротрансмиттеры.
Когда электрический нервный импульс или потенциал действия достигает конца пресинаптического нейрона, это заставляет синаптические пузырьки — крошечные мембранные « пакеты », содержащие нейротрансмиттеры — сливаться с терминальной мембраной, высвобождая нейротрансмиттеры в промежуток между ними. нейроны.Когда постсинаптический нейрон воспринимает достаточное количество нейротрансмиттеров, это запускает новый потенциал действия в постсинаптическом нейроне.
Отделение CMSF использовало срезы мозга крысы для изучения гигантского синапса, называемого чашечкой Хельда. Ученые индуцировали электрические сигналы на разных частотах, а затем обнаружили потенциалы действия, генерируемые в постсинаптическом нейроне. Они обнаружили, что по мере увеличения частоты электрических сигналов изофлуран оказывал более сильное влияние на блокировку передачи.
Чтобы подтвердить выводы своего подразделения, Такахаши обратился к доктору Такаюки Ямасите, исследователю из Университета Нагоя, который проводил эксперименты с синапсами, называемыми кортико-кортикальными синапсами, в мозге живых мышей.
Ямасита обнаружил, что анестетик воздействует на корково-корковые синапсы так же, как на чашечку Хельда. Когда мышей анестезировали изофлураном, высокочастотная передача сильно снижалась, в то время как влияние на низкочастотную передачу было меньше.
«Оба этих эксперимента подтвердили, что изофлуран действует как общий анестетик», — сказал Такахаши. «Но мы хотели понять, какие механизмы, лежащие в основе изофлурана, нацелены на ослабление синапсов таким частотно-зависимым образом».
Достижение целей
В ходе дальнейших исследований исследователи обнаружили, что изофлуран снижает количество высвобождаемого нейромедиатора как за счет снижения вероятности высвобождения пузырьков, так и за счет уменьшения максимального количества пузырьков, которые могут высвобождаться за один раз.
Таким образом, ученые исследовали, влияет ли изофлуран на ионные каналы кальция, которые играют ключевую роль в процессе высвобождения везикул. Когда потенциалы действия достигают пресинаптического окончания, каналы для ионов кальция в мембране открываются, позволяя ионам кальция проникать внутрь. Затем синаптические везикулы обнаруживают это повышение уровня кальция и сливаются с мембраной. Исследователи обнаружили, что изофлуран снижает приток кальция, блокируя каналы ионов кальция, что, в свою очередь, снижает вероятность высвобождения везикул.
«Однако этот механизм сам по себе не может объяснить, как изофлуран снижает количество высвобождаемых пузырьков или частотно-зависимую природу эффекта изофлурана», — сказал Такахаши.
Ученые предположили, что изофлуран может уменьшить количество высвобождаемых везикул, либо напрямую блокируя процесс высвобождения везикул путем экзоцитоза, либо косвенно блокируя рециклинг везикул, когда везикулы реформируются за счет эндоцитоза, а затем наполняются нейротрансмиттером, готовым к повторному высвобождению.
Путем электрического измерения изменений площади поверхности пресинаптической терминальной мембраны, которая увеличивается за счет экзоцитоза и уменьшается за счет эндоцитоза, ученые пришли к выводу, что изофлуран влияет только на высвобождение везикул за счет экзоцитоза, вероятно, за счет блокировки экзоцитоза.
«Важно отметить, что мы обнаружили, что этот блок оказывает сильное влияние только на высокочастотные сигналы, предполагая, что этот блок на экзоцитарном механизме является ключом к анестезирующему эффекту изофлурана», — сказал Такахаши.
Ученые предположили, что высокочастотные потенциалы действия вызывают такой массовый приток кальция в пресинаптический терминал, что изофлуран не может эффективно снижать концентрацию кальция. Таким образом, синаптическая сила ослабляется преимущественно прямым блоком экзоцитарного аппарата, а не снижением вероятности высвобождения везикул.
Между тем, низкочастотные импульсы вызывают меньший экзоцитоз, поэтому блокировка изофлурана на экзоцитозный механизм оказывает незначительное влияние.Хотя изофлуран эффективно снижает поступление кальция в пресинаптический терминал, само по себе снижение вероятности высвобождения везикул недостаточно для блокирования постсинаптических потенциалов действия в чашечке Held и оказывает лишь незначительное влияние на кортико-кортикальные синапсы. Таким образом сохраняется низкочастотная передача.
В целом, серия экспериментов предоставляет убедительные доказательства того, как изофлуран ослабляет синапсы, вызывая анестезию.
«Теперь, когда мы разработали методы манипулирования и расшифровки пресинаптических механизмов, мы готовы применять эти методы для решения более сложных вопросов, таких как пресинаптические механизмы, лежащие в основе симптомов нейродегенеративных заболеваний», — сказал Такахаши.«Это будет нашим следующим вызовом».
Вопрос исследования: Как действует анестезия?
Эрик Мендес
Многие изобретения XIX века — телефоны, самолеты, фонографы — помогли сформировать наш современный мир. Однако можно утверждать, что открытие в 1846 году эффективной хирургической анестезии занимает почетное место среди достижений века. До появления эффективных анестетиков операция была крайней крайней мерой, в которой использовались грубые и опасные средства (в том числе большие дозы опиума или алкоголя или сбивание пациента без сознания) для притупления ощущений пациента.Сегодня, будь то укол новокаина у стоматолога, спинальная или эпидуральная анестезия во время родов, глубокая седация для небольшой процедуры или общая анестезия для серьезной операции, использование эффективной анестезии является обычной частью нашей медицинской помощи.
Хотя большинство из нас испытали анестезию, широкая публика мало понимает, что это такое и как работает.
По словам Стива Киматиана, доцента кафедры анестезиологии и педиатрии Медицинского колледжа Пенсильванского университета, анестезия — это не единое целое, а скорее манипуляция несколькими физиологическими функциями организма.
«В самом общем смысле вы можете сказать, что анестезия состоит из четырех компонентов: гипноза, амнезии, обезболивания и расслабления мышц», — объясняет Киматиан.
Эти компоненты — от инъекций местного анестетика до регионарной анестезии (например, спинальной и эпидуральной) до общей анестезии — можно комбинировать или использовать по отдельности в зависимости от типа операции и потребностей пациента.
В подростковом возрасте вы, возможно, думали, что «спите» после тонзиллэктомии, но формально вы находились в состоянии глубокого гипноза.Когда вы наконец проснулись в палате для восстановления, вы, вероятно, ничего не помнили об операции — благодаря действию препаратов, вызывающих амнезию, которые вам были введены.
Но Киматиан объясняет, что седация и амнезия не обязательно означают одно и то же. Вы можете «спать» во время процедуры, но потом помните, что слышите голоса врачей, или вы также можете «бодрствовать» во время процедуры, разговаривая с врачами, отвечая на вопросы и следуя командам, но ничего не запоминая.
По словам Киматиана, хотя вы не помните, чтобы во время операции была какая-либо боль, это не обязательно означает, что боли не было.
«Человек может быть под воздействием седативных препаратов и казаться спящим, он может быть в амнезии и ничего не помнить, но его тело все еще может иметь физиологический ответ на раздражитель» «Рассмотрим аналогию с падением дерева в лесу. Если у вас была боль и вы не помните, действительно ли у вас была боль? С точки зрения анестезиолога, да, потому что мы должны учитывать те физиологические изменения, которые происходят в ответ на раздражитель.«
В случаях, когда требуется регионарная анестезия, как анестезиологи блокируют чувствительность определенных частей тела, а не других?
Как поясняет Киматиан, если мы дотрагиваемся до горячей плиты, тепловые рецепторы в нашей руке посылают электрический сигнал в наш спинной мозг, который сигнализирует нашему мозгу, и мы реагируем, испытывая боль и убирая руку от раздражителя. Чтобы убедиться, что мы не чувствуем боли во время операции или процедуры, анестезиолог использует анальгетики или местные анестетики, чтобы заблокировать сигнал где-то между точкой раздражителя и мозгом.
«Я мог бы сделать регионарную анестезию выборочно для отдельного пальца, просто заблокировав нервы этого пальца, и вы не заметили бы, что палец болит», — говорит Киматиан. «Или вы можете заблокировать все нервы к предплечью, чтобы не чувствовать там боли. Можно заблокировать его в плече. Вы можете заблокировать его в эпидуральном пространстве, где нервы входят в спинной мешок, или вы можете положить человек полностью уснул и заблокировал его на церебральном уровне ». По словам Киматиана, искусство и наука анестезии заключается в том, чтобы адаптировать как технику, так и дозировку к индивидуальным потребностям пациента.«Понимание тонкого баланса между желаемыми эффектами и нежелательными побочными эффектами требует от врача глубоких знаний физиологии и фармакологии», — добавляет он.
Стивен Киматиан, доктор медицинских наук, FAAP, доцент кафедры анестезиологии и педиатрии, а также директор программы резидентуры по анестезиологии в Медицинском центре Милтона С. Херши. С ним можно связаться по адресу [email protected].
Общая анестезия перехватывает схему сна, чтобы вырубить вас
Открытие общей анестезии 170 лет назад стало медицинским чудом, позволив миллионам пациентов безболезненно перенести инвазивные, спасающие жизнь операции.Тем не менее, несмотря на десятилетия исследований, ученые до сих пор не понимают, почему работает общая анестезия.
Теперь ученые думают, что они открыли часть ответа. В исследовании, опубликованном 18 апреля в сети Neuron, команда из Университета Дьюка обнаружила, что несколько разных препаратов для общей анестезии выводят вас из строя, захватывая нервную систему, которая заставляет вас засыпать.
Исследователи проследили эту нейронную схему до крошечного кластера клеток в основании мозга, ответственного за выработку гормонов, регулирующих функции организма, настроение и сон.Это одно из первых открытий, предполагающих роль гормонов в поддержании состояния общей анестезии, и дает ценную информацию для создания новых лекарств, которые могут усыпить людей с меньшими побочными эффектами.
С тех пор, как первый пациент прошел под общим наркозом в 1846 году, ученые пытались выяснить, как именно это работает. Преобладала теория, что многие из этих препаратов подавляют нормальную деятельность мозга, что приводит к неспособности двигаться или чувствовать боль.Подобные теории вращались вокруг сна, родственного состояния общей анестезии. Однако исследования последнего десятилетия показали, что сон — более активный процесс, чем считалось ранее, когда целые наборы нейронов работают, пока вы ловите свои Z.
Фань Ван, доктор философии, профессор нейробиологии медицинского факультета Университета Дьюка, и Ли-Фэн Цзян-Се, аспирантка в ее лаборатории, задались вопросом, является ли преобладающее мнение об общей анестезии также односторонним.«Возможно, вместо того, чтобы просто подавлять нейроны, анестетики могут активировать определенные нейроны в головном мозге», — сказал Цзян-Се.
Чтобы проверить свою новую теорию, Цзян-Се и Лупин Инь, доктор философии, научный сотрудник лаборатории Ванга, подвергли мышей общей анестезии несколькими различными, но обычно используемыми лекарствами. Затем они использовали молекулярные маркеры, чтобы отследить нейроны, которые обычно активировались анестетиками. Они обнаружили группу активно возбуждающих нейронов, похороненных в крошечной области мозга, называемой супраоптическим ядром, которое, как известно, имеет длинные выступы, которые выделяют большое количество гормонов, таких как вазопрессин, непосредственно в кровоток.
«Большинство активированных анестезией клеток были своего рода гибридными клетками, которые соединяют нервную систему и эндокринную систему», — сказал Цзян-Се. «Это застало нас врасплох и привело к неизведанной территории для понимания нервных путей общей анестезии».
Затем исследователи применили сложную технику, разработанную в лаборатории Ванга, для включения или выключения этой специализированной группы клеток с помощью химических веществ или света. Когда они включали клетки у мышей, животные перестали двигаться и впадали в глубокий сон, называемый медленным сном, обычно связанный с потерей сознания.
Затем группа исследователей уничтожила эту группу клеток. Мыши продолжали передвигаться, не имея возможности заснуть.
Наконец, исследователи провели аналогичные эксперименты на мышах под общим наркозом. Они обнаружили, что искусственная предварительная активация нейроэндокринных клеток заставляла мышей оставаться под общей анестезией в течение более длительных периодов времени. И наоборот, когда они заставили эти клетки замолчать, мыши легче просыпались от анестезии.
Это исследование также выявило ранее неожиданную роль клеток мозга, секретирующих гормоны, в обеспечении глубокого сна.
«Многие люди, особенно страдающие болезнью Альцгеймера, испытывают трудности с засыпанием, однако современные лекарства имеют неприятные побочные эффекты», — сказал Инь. «Если мы сможем найти способы манипулировать этой нейронной схемой, возможно, путем нацеливания на гормоны или небольшие пептиды, то это может привести к разработке лучших снотворных».
Исследование было поддержано грантами Фонда В. М. Кека, Фонда исследований мозга и Национальных институтов здравоохранения (DP1Mh203908), а также научным сообществом Human Frontier Science Fellowship (LT000038 / 2018-L).
ЦИТАТА: «Общий нейроэндокринный субстрат для различных общих анестетиков и сна», Ли-Фэн Цзян-Се, Лупин Инь, Шэнли Чжао, Винсент Превосто, Бао-Ся Хан, Кафуй Дзираса и Фань Ван. Neuron, 5 июня 2019 г. (онлайн-версия, 18 апреля 2019 г.). DOI: 10.1016 / j.neuron.2019.03.033
Это то, что обезболивающее влияет на ваш мозг
Большинству из нас в какой-то момент жизни будет проведена общая анестезия, чтобы врачи могли оперировать нас, не чувствуя ничего, но как именно это удерживает нас в бессознательном состоянии из-за серьезной боли? Честно говоря, ученые не совсем уверены, как это работает, как объясняется в этом выпуске SciShow.Но они знают, что происходит с нашим мозгом, когда им вводят анестетик, и результаты довольно крутые.
Начнем с того, что обычно есть два препарата, которые используются для того, чтобы подвергнуть вас общей анестезии: первое быстро вырубает вас, а второе удерживает вас в таком состоянии на протяжении всей операции.
Доза этого второго препарата — это та, с которой работают анестезиологи, чтобы убедиться, что мы не просыпаемся слишком рано или не погружаемся слишком глубоко. Идеального количества достаточно, чтобы мы просыпались без воспоминаний о том, что только что было сделано с нашим телом.
Но даже несмотря на то, что нахождение под наркозом часто похоже на глубокий сон без сновидений, сканирование мозга показало, что этот процесс на самом деле не похож на сон. Мало того, что разные области мозга активируются, они также не общаются друг с другом под наркозом, как обычно, когда вы спите.
Более того, под наркозом нет быстрого движения глаз, а мозговые волны очень похожи на мозговые волны пациентов в коме, как объясняет Хэнк Грин в видео.

